
°æƒø°ø‘⁄Œ¬∂»°¢»›ª˝œ‡Õ¨µƒ3∏ˆ√‹±’»›∆˜÷–£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨±£≥÷∫„Œ¬°¢∫„»›£¨≤‚µ√∑¥”¶¥ÔµΩ∆Ω∫‚ ±µƒ”–πÿ ˝æ›»Áœ¬£®“—÷™![]()
![]() kJ°§mol
kJ°§mol![]() £©œ¬¡–Àµ∑®’˝»∑µƒ «
£©œ¬¡–Àµ∑®’˝»∑µƒ «
»›∆˜ | º◊ | ““ | ±˚ |
∑¥”¶ŒÔÕ∂»Î¡ø | 1mol N2°¢3mol H2 | 2mol NH3 | 4mol NH3 |
NH3µƒ≈®∂»£®mol°§L | c1 | c2 | c3 |
∑¥”¶µƒƒ‹¡ø±‰ªØ | ∑≈≥ˆakJ | Œ¸ ’bkJ | Œ¸ ’ckJ |
ÃÂœµ—π«ø£®Pa£© | p1 | p2 | p3 |
∑¥”¶ŒÔ◊™ªØ¬ |
|
|
|
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
°æ¥∞∏°øB
°æΩ‚Œˆ°ø
º◊»›∆˜∑¥”¶ŒÔÕ∂»Î1molN2°¢3molH2£¨““»›∆˜∑¥”¶ŒÔÕ∂»Î¡ø2molNH3£¨∫„Œ¬«“““»›∆˜»›ª˝∫Õº◊»›∆˜œ‡Õ¨£¨‘Úº◊»›∆˜”Γ“»›∆˜ «µ»–ß∆Ω∫‚£ªº◊»›∆˜∑¥”¶ŒÔÕ∂»Î1molN2°¢3molH2£¨±˚»›∆˜∑¥”¶ŒÔÕ∂»Î¡ø4molNH3£¨≤…”√º´œfi◊™ªØ∑®◊™ªØŒ™∑¥”¶ŒÔŒ™2molN2°¢6molH2£¨ «º◊÷–µƒ∂˛±∂£¨»Áπ˚∫„Œ¬«“±˚»›∆˜»›ª˝ «º◊»›∆˜2±∂£¨‘Úº◊»›∆˜”α˚»›∆˜“≤ «µ»–ß∆Ω∫‚£ªÀ˘“‘±˚À˘µΩ¥Ôµƒ∆Ω∫‚£¨ø…“‘ø¥◊˜‘⁄∫„Œ¬«“»›ª˝ «º◊»›∆˜¡Ω±∂Ãıº˛œ¬£¨µΩ¥Ô∆Ω∫‚∫Û£¨‘Ÿ—πÀıê˝Œ™”κ◊»›∆˜Ãª˝œ‡µ»À˘µΩ¥Ôµƒ∆Ω∫‚£ªæ›¥À∑÷Œˆ∆Ω∫‚“∆∂Ø°£
º◊Õ∂»Î1molN2°¢3molH2£¨““»›∆˜Õ∂»Î¡ø2molNH3£¨∫„Œ¬∫„»›Ãıº˛œ¬£¨º◊»›∆˜”Γ“»›∆˜ «µ»–ß∆Ω∫‚£¨∏˜◊È∑÷µƒŒÔ÷ µƒ¡ø°¢∫¨¡ø°¢◊™ªØ¬ µ»ÕÍ»´œ‡µ»£ª∂¯º◊»›∆˜Õ∂»Î1molN2°¢3molH2£¨±˚»›∆˜º”»Î4molNH3£¨≤…”√º´œfi◊™ªØ∑®±˚œ‡µ±”⁄º”»Î2molN2°¢6molH2£¨±˚÷–º”»Î¡ø «º◊÷–µƒ∂˛±∂£¨»Áπ˚∫„Œ¬«“±˚»›∆˜»›ª˝ «º◊»›∆˜2±∂£¨‘Úº◊»›∆˜”α˚»›∆˜Œ™µ»–ß∆Ω∫‚£¨À˘“‘±˚À˘µΩ¥Ôµƒ∆Ω∫‚£¨ø…“‘ø¥◊˜‘⁄∫„Œ¬«“»›ª˝ «º◊»›∆˜¡Ω±∂Ãıº˛œ¬£¨µΩ¥Ô∆Ω∫‚∫Û£¨‘Ÿ—πÀıê˝Œ™”κ◊»›∆˜Ãª˝œ‡µ»À˘µΩ¥Ôµƒ∆Ω∫‚£¨”…”⁄∏√∑¥”¶ «Ãª˝ºı–°µƒ∑¥”¶£¨Àı–°»›∆˜Ãª˝£¨‘ˆ¥Û¡À—π«ø£¨∆Ω∫‚œÚ◊≈’˝œÚ“∆∂Ø£¨À˘“‘±˚÷–µ™∆¯°¢«‚∆¯◊™ªØ¬ ¥Û”⁄º◊∫Õ““µƒ°£
A.±˚»›∆˜∑¥”¶ŒÔÕ∂»Î¡ø4molNH3£¨≤…”√º´œfi◊™ªØ∑®◊™ªØŒ™∑¥”¶ŒÔŒ™2molN2°¢6molH2£¨ «º◊÷–µƒ∂˛±∂£¨»Ù∆Ω∫‚≤ª“∆∂Ø£¨c3=2c1£ª±˚œ‡µ±”⁄‘ˆ¥Û—π«ø£¨∆Ω∫‚œÚ◊≈’˝œÚ“∆∂Ø£¨À˘“‘±˚÷–∞±∆¯µƒ≈®∂»¥Û”⁄““÷–∞±∆¯≈®∂»µƒ∂˛±∂£¨º¥c3£æ2c1£¨π A¥ÌŒÛ£ª
B.º◊Õ∂»Î1molN2°¢3molH2£¨““÷–Õ∂»Î2molNH3£¨‘Úº◊”Γ“ «ÕÍ»´µ»–ßµƒ£¨∏˘æ›∏«Àπ∂®¬…ø…÷™£¨º◊”Γ“µƒ∑¥”¶µƒƒ‹¡ø±‰ªØ÷Æ∫ÕŒ™92.4kJ£¨π a+b=92.4£¨π B’˝»∑£ª
C.±˚»›∆˜∑¥”¶ŒÔÕ∂»Î¡ø4molNH3£¨ «““µƒ∂˛±∂£¨»Ù∆Ω∫‚≤ª“∆∂Ø£¨±˚÷–—π«øŒ™““µƒ∂˛±∂;”…”⁄±˚÷–œ‡µ±”⁄‘ˆ¥Û—π«ø£¨∆Ω∫‚œÚ◊≈œÚ◊≈’˝œÚ“∆∂Ø£¨À˘“‘±˚÷–—π«øºı–°£¨–°”⁄““µƒ2±∂£¨º¥2p2£æp3£¨π C¥ÌŒÛ£ª
D.±˚»›∆˜∑¥”¶ŒÔÕ∂»Î¡ø4molNH3£¨ «““µƒ∂˛±∂£¨»Ù∆Ω∫‚≤ª“∆∂Ø£¨◊™ªØ¬ ¶¡1+¶¡3=1£ª”…”⁄±˚÷–œ‡µ±”⁄‘ˆ¥Û—π«ø£¨∆Ω∫‚œÚ◊≈œÚ◊≈’˝œÚ“∆∂Ø£¨∞±∆¯µƒ◊™ªØ¬ ºı–°£¨À˘“‘◊™ªØ¬ ¶¡1+¶¡3£º1£¨π D¥ÌŒÛ°£
π —°B°£


 ”≈µ»…˙Âø‚œµ¡–¥∞∏
”≈µ»…˙Âø‚œµ¡–¥∞∏
| ƒÍº∂ | ∏fl÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏fl“ª | ∏fl“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl∂˛ | ∏fl∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl»˝ | ∏fl»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“‘∏ıÃ˙øÛ(÷˜“™≥…∑÷Œ™FeO∫ÕCr2O3£¨∫¨”–Al2O3°¢SiO2µ»‘”÷ )Œ™÷˜“™‘≠¡œ…˙≤˙ªØπ§‘≠¡œ∫Ï∑؃∆(÷˜“™≥…∑÷Na2Cr2O7°§2H2O)£¨∆‰÷˜“™π§“’¡˜≥ûÁœ¬£∫

≤È‘ƒ◊ ¡œµ√÷™:
¢°£Æ≥£Œ¬œ¬£¨NaBiO3≤ª»‹”⁄ÀÆ£¨”–«ø—ıªØ–‘£¨‘⁄ºÓ–‘Ãıº˛œ¬£¨ƒ‹Ω´Cr3+◊™ªØŒ™CrO42£≠°£
¢¢£Æ
Ω Ù¿Î◊” | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
ø™ º≥¡µÌµƒpH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
≥¡µÌÕÍ»´µƒpH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
ªÿ¥œ¬¡–Œ £∫
£®1£©∑¥”¶÷Æ«∞œ»Ω´øÛ Ø∑€Àȵƒƒøµƒ «__________________°£
£®2£©≤Ω÷Ë¢€º”µƒ ‘º¡Œ™_____________£¨¥À ±»‹“∫pH“™µ˜µΩ5µƒƒøµƒ_______________ °£
£®3£©–¥≥ˆ∑¥”¶¢‹µƒ¿Î◊”∑¥”¶∑Ω≥à Ω______________________°£
£®4£©¢›÷–À·ªØ « πCrO42£≠◊™ªØŒ™Cr2O72£≠£¨–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥à Ω_________________°£
£®5£©Ω´»‹“∫Hæ≠π˝’Ù∑¢≈®Àı£¨¿‰»¥Ω·æߣ¨π˝¬À£¨œ¥µ”£¨∏…‘Ôº¥µ√∫Ï∑؃∆¥÷æßã¨æ´÷∆∫Ï∑؃∆‘Ú∂‘¥÷æßÖ˓™≤…”√µƒ≤Ÿ◊˜ «__________________(ÃÓ≤Ÿ◊˜√˚≥∆)°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øƒ≥ªØπ§≥ß…˙≤˙µƒ∆Ø∞◊∑€£¨≤˙∆∑Àµ√˜ È»Áœ¬£∫

«Îƒ„ªÿ¥£∫
(1)«Îƒ„Œ™∆Ø∞◊∑€–¥“ª∑›±£¥Ê°¢ π”√µƒ◊¢“‚ ¬œÓ(≤ª≥¨π˝30◊÷)°£____°£
(2)”√ªØ—ß∑Ω≥Ã Ω±Ì æ£∫
¢Ÿ∆Ø∞◊∑€µƒ…˙≤˙‘≠¿Ì£∫_____________________________
¢⁄“ª∞„«Èøˆœ¬£¨∆Ø∞◊∑€ ß–ßµƒ÷˜“™‘≠“Ú£∫____________£ª______°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øµÕŒ¬Õ—œıºº ıø…”√”⁄¥¶¿Ì∑œ∆¯÷–µƒµ™—ıªØŒÔ£¨∑¢…˙µƒªØ—ß∑¥”¶Œ™2NH3(g)£´NO(g)£´NO2(g)![]() 2N2(g)£´3H2O(g) ¶§H<0°£‘⁄∫„»›µƒ√‹±’»›∆˜÷–£¨œ¬¡–”–πÿÀµ∑®’˝»∑µƒ «
2N2(g)£´3H2O(g) ¶§H<0°£‘⁄∫„»›µƒ√‹±’»›∆˜÷–£¨œ¬¡–”–πÿÀµ∑®’˝»∑µƒ «
A. ∆‰À˚Ãıº˛≤ª±‰£¨ π”√∏fl–ߥflªØº¡£¨ª·Àı∂Ã∑¥”¶ ±º‰«“∑œ∆¯÷–µ™—ıªØŒÔµƒ◊™ªØ¬ ‘ˆ¥Û
B. ∆‰À˚Ãıº˛≤ª±‰£¨º”»Î◊„¡øµƒNH3£¨‘Ÿ¥Œ∆Ω∫‚∫Ûµ™—ıªØŒÔµƒ◊™ªØ¬ ‘ˆ¥Û£¨µ™∆¯µƒÃª˝∑÷ ˝ºı–°
C. ∆‰À˚Ãıº˛≤ª±‰£¨…˝∏flŒ¬∂»ª·Ã·∏fl∑¥”¶ŒÔµƒ◊™ªØ¬ «“ π∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝‘ˆ¥Û
D. ∆‰À˚Ãıº˛≤ª±‰£¨Àı–°»›∆˜µƒÃª˝ª· π∆Ω∫‚’˝œÚ“∆∂Ø£¨‘Ÿ¥Œ∆Ω∫‚∫Û∞±∆¯µƒ≈®∂»±‰–°
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“ª∂®Ãıº˛œ¬£¨ø…ƒÊ∑¥”¶X£®g£©£´3Y£®g£©![]() 2Z£®g£©°˜H <0£¨»ÙX°¢Y°¢Z∆ º≈®∂»∑÷±Œ™c1°¢c2°¢c3£®æ˘≤ªŒ™0£©£¨µ±¥Ô∆Ω∫‚ ±X°¢Y°¢Zµƒ≈®∂»∑÷±Œ™0.2mol /L£¨0.6mol/ L£¨0.1 mol/L£¨‘Úœ¬¡–≈–∂œ≤ª∫œ¿Ìµƒ «
2Z£®g£©°˜H <0£¨»ÙX°¢Y°¢Z∆ º≈®∂»∑÷±Œ™c1°¢c2°¢c3£®æ˘≤ªŒ™0£©£¨µ±¥Ô∆Ω∫‚ ±X°¢Y°¢Zµƒ≈®∂»∑÷±Œ™0.2mol /L£¨0.6mol/ L£¨0.1 mol/L£¨‘Úœ¬¡–≈–∂œ≤ª∫œ¿Ìµƒ «
A. ∆ º ±c1£∫c2£Ω1£∫3«“ ∆Ω∫‚ ±X°¢Yµƒ◊™ªØ¬ œ‡µ»
B. c1µƒ»°÷µ∑∂ŒßŒ™0< c1<0£Æ25mo /L
C. ∑¥”¶ø™ º∫Û£¨Y∫ÕZµƒ…˙≥…ÀŸ¬ ÷Ʊ»Œ™2£∫3
D. ∂‘∆Ω∫‚ÃÂœµº”»»£¨‘ÚªÏ∫Õ∆¯Ãµƒ∆Ωæ˘∑÷◊”¡øºı–°
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øƒ≥¿Î◊”∑¥”¶…ʺ∞µΩClO©Å°¢NH4+°¢N2°¢Cl©Åµ»Œ¢¡££¨∆‰÷–N2°¢ClO£≠µƒŒÔ÷ µƒ¡øÀÊ ±º‰±‰ªØµƒ«˙œfl»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
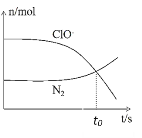
A. ∏√∑¥”¶÷–ClO£≠Œ™—ıªØº¡£¨N2Œ™—ıªØ≤˙ŒÔ
B. ∑¥”¶∫Û»‹“∫µƒpHºı–°
C. »ÁÕºt0 ±∑¥”¶¥Ô∆Ω∫‚◊¥Ã¨
D. ∑¥”¶π˝≥Ã÷–√ø…˙≥…1 mol N2£¨◊™“∆6molµÁ◊”
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø”–A°¢B°¢C°¢D°¢EŒÂ÷÷∂Ã÷‹∆⁄‘™Àÿ£¨“—÷™œ‡¡⁄µƒA°¢B°¢C°¢DÀƒ÷÷‘™Àÿ‘≠◊”∫ÀÕ‚π≤”–56∏ˆµÁ◊”£¨‘⁄÷‹∆⁄±Ì÷–µƒŒª÷√»ÁÕºÀ˘ æ°£Eµƒµ•÷ ø…”ÎÀ·∑¥”¶£¨1 mol Eµ•÷ ”Î◊„¡øÀ·◊˜”√£¨‘⁄±Í◊º◊¥øˆœ¬ƒ‹≤˙…˙33.6 L H2£ªEµƒ—Ù¿Î◊””ÎAµƒ“ı¿Î◊”∫ÀÕ‚µÁ◊”≤„Ω·ππÕÍ»´œ‡Õ¨£¨ªÿ¥œ¬¡–Œ £∫

(1)ŒÂ÷÷‘™Àÿµƒ√˚≥∆£∫A________£¨B________£¨C________£¨D________£¨E________°£
(2)ª≠≥ˆC‘≠◊”°¢A¿Î◊”µƒΩ·ππ æ“‚Õº£∫__________________°¢__________________°£
(3)Bµ•÷ ‘⁄Dµ•÷ ÷–»º…’£¨∑¥”¶œ÷œÛ «_______________________£¨…˙≥…ŒÔµƒªØ—ß ΩŒ™_____________________°£
(4)A”ÎE–Œ≥…ªØ∫œŒÔµƒªØ—ß ΩŒ™______________£¨À¸µƒ–‘÷ æˆ∂®¡ÀÀ¸‘⁄ŒÔ÷ µƒ∑÷¿‡÷–”¶ Ù”⁄__________________°£
(5)œÚD”ÎE–Œ≥…µƒªØ∫œŒÔµƒÀÆ»‹“∫÷–µŒ»Î…’ºÓ»‹“∫÷±÷¡Œfi√˜œ‘œ÷œÛ∑¢…˙ ±£¨π€≤ÏµΩµƒœ÷œÛ «œ»”–∞◊…´Ω∫◊¥≥¡µÌ≤˙…˙≤¢÷Ω•‘ˆ∂‡£¨ÀÊNaOHº”»Î”÷÷Ω•»‹Ω‚◊Ó÷’≥Œ«Â£¨«Î–¥≥ˆ”–πÿ∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™_______________________°¢___________________________________________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–±»Ωœ÷–£¨’˝»∑µƒ «£® £©
A. Õ¨Œ¬∂»Õ¨ŒÔ÷ µƒ¡ø≈®∂» ±£¨HF±»HCN“◊µÁ¿Î£¨‘ÚNaF»‹“∫µƒpH±»NaCN»‹“∫¥Û
B. 0.2 mol°§L-1NH4Cl∫Õ0.1 mol°§L-1NaOH»‹“∫µ»Ãª˝ªÏ∫œ∫Û£∫c(![]() )£æc(Cl-)£æc(Na+)£æc(OH-)£æc(H+)
)£æc(Cl-)£æc(Na+)£æc(OH-)£æc(H+)
C. ŒÔ÷ µƒ¡ø≈®∂»œ‡µ»µƒH2S∫ÕNaHSªÏ∫œ»‹“∫÷–£∫c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. Õ¨≈®∂»µƒœ¬¡–»‹“∫÷–£¨¢Ÿ(NH4)2SO4°¢¢⁄NH4Cl°¢¢€CH3COONH4°¢¢‹NH3°§H2O£ªc(![]() )”…¥ÛµΩ–°µƒÀ≥–Ú «£∫¢Ÿ£æ¢⁄£æ¢€£æ¢‹
)”…¥ÛµΩ–°µƒÀ≥–Ú «£∫¢Ÿ£æ¢⁄£æ¢€£æ¢‹
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø(1)«¶–ÓµÁ≥ÿ «≥£”√µƒªØ—ßµÁ‘¥£¨∆‰µÁº´≤ƒ¡œ «Pb∫ÕPbO2£¨µÁΩ‚“∫Œ™œ°¡ÚÀ·°£π§◊˜ ±∏√µÁ≥ÿ◊‹∑¥”¶ ΩŒ™£∫Pb+PbO2 +2H2SO4=2PbSO4+2H2O£¨æ›¥À≈–∂œ£∫
¢Ÿ«¶–ÓµÁ≥ÿµƒ∏∫º´≤ƒ¡œ «________£®–¥ªØ—ß Ω£©£ª
¢⁄π§◊˜ ±’˝º´∑¥”¶Œ™__________________________________________£ª
¢€π§◊˜ ±£¨µÁΩ‚÷ »‹“∫÷–“ı¿Î◊”“∆œÚ________º´(ÃÓ°∞’˝°±ªÚ°∞∏∫°±)°£
(2)»ÁÕºA ÷±¡˜µÁ‘¥£¨BŒ™Ω˛Õ∏±•∫Õ¬»ªØƒ∆»‹“∫∫Õ∑”Ù ‘“∫µƒ¬À÷Ω£¨CŒ™µÁ∂∆≤€£¨Ω”Õ®µÁ¬∑∫Û£¨∑¢œ÷B…œµƒcµ„œ‘∫Ï…´£¨«ÎÃÓø’£∫

¢ŸµÁ‘¥A…œµƒaŒ™________º´(ÃÓ°∞’˝°±ªÚ°∞∏∫°±)£ª
¢⁄¬À÷ΩB…œ∑¢…˙µƒ◊‹ªØ—ß∑Ω≥Ã ΩŒ™___________________£ª
¢€”˚‘⁄µÁ≤€÷– µœ÷Ã˙…œ∂∆–ø£¨Ω”Õ®Kµ„£¨ πc°¢d¡Ωµ„∂ì∑£¨‘ÚµÁº´f…œ∑¢…˙µƒ∑¥”¶Œ™________________________°£µÁ≤€÷–∑≈µƒ∂∆“∫ø…“‘ «___________(÷ª–Ë–¥≥ˆ“ª÷÷º¥ø…)°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒfi÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com