
【题目】(1)今有反应2H2+O2===2H2O,要构成燃料电池,则负极通入的应是________,正极通入的应是 ________,电极反应式分别为负极:__________________________、正极:________________。
(2)如把KOH改为稀H2SO4作电解液,则电极反应式分别为负极:__________、正极:______。
(3)如把H2改为甲烷,KOH溶液作电解液,则负极反应式为:______________________________。
【答案】 H2 O2 2H2+4OH--4e-===4H2O O2+2H2O+4e-===4OH- 2H2-4e-===4H+ O2+4H++4e-===2H2O CH4+10OH--8e-===CO![]() +7H2O
+7H2O
【解析】(1)根据电池反应式可知在反应中H2被氧化,O2被还原.H2应该在负极上反应,O2应该在正极上反应,又因为是碱性溶液,不可能有H+参加或生成,故负极的电极反应为H2-2e-+2OH-=2H2O,正极的电极反应为O2+2H2O+4e-=4OH-,故答案为:H2;O2;H2-2e-+2OH-=2H2O;O2+2H2O+4e-=4OH-;
(2)若将电解质溶液换为酸性溶液,此时应考虑不可能有OH-生成,故负极的电极反应为H2-2e-=2H+,正极的电极反应为O2+4H++4e-=2H2O,故答案为:H2-2e-=2H+;O2+4H++4e-=2H2O;
(3)如把H2改为甲烷,KOH溶液做电解质,氧气在正极得到电子生成氢氧根离子,则正极为2O2+4H2O+8e-=8OH-,甲烷失电子在碱溶液中反应,甲烷在负极失电子发生氧化反应在碱溶液中生成碳酸盐,此时不会有CO2放出;负极为CH4+10OH--8e-=CO32-+7H2O,故答案为:CH4+10OH--8e-=CO32-+7H2O。


科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分:

(1)元素⑩原子结构示意图为__________.
(2)元素③④的第一电离能大小关系为_______(填化学用语,下同),原因是__________________。④-⑧中最高价氧化物对应水化物酸性最强的是_______.
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式_________。
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是__________(用元素符号表示),下列表述中能证明这一事实的是__________。
A.气态氢化物的挥发性和稳定性
B.两元素的电负性
C.单质分子中的键能
D.含氧酸的酸性
E.氢化物中X—H键的键长
F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①T元素最可能是________(填“s”、“p”、“d”、“ds”等)区元素;
在周期表中,最可能处于同一主族的是_________.(填元素代号),
②下列离子的氧化性最弱的是______________。
A.S2+ B.R2+ C.U+ D.T3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)C中官能团的名称为:_______。
(4)由C生成D的化学方程式:___________________________________。
(5)由C生成E的化学方程式:___________________________________。
(6)已知F是A的同系物,F的相对分子质量比A多28,则与F互为同分异构体且能发生银镜反应的结构种类有_____________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的Na+的物质的量浓度(单位:mol·L-1)为
A. (y-2x)/a B. (y-x)/a C. (2y-4x)/a D. (2y-2x)/a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统。其工作原理如图所示。以下说法中错误的是( )

A.电池的负极反应为:Mg-2e-===Mg2+
B.电池工作时,H+向负极移动
C.电池工作一段时间后,溶液的pH增大
D.电池总反应式是:Mg+H2O2+2H+===Mg2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p轨道电子数比s轨道电子数少1,C为金属元素且原子核外p轨道电子数和s轨道电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出四种元素的元素符号:A_______,B_______,C_______,D_______。
(2)写出C、D两种基态原子核外电子排布图:
C________________________________________________________________________;
D________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子性质的解释中,不正确的是
A. 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键
B. 乳酸有一对对映异构体,因为其分子中含有一个手性碳原子
C. 碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”解释
D. 由右图可知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 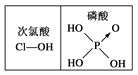
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
罗氟司特是用于治疗慢性阻塞性肺病的新型药物,可通过以下方法合成:
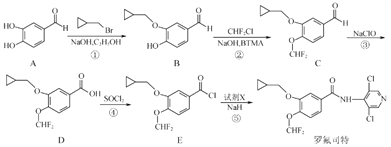
(1)化合物C中的含氧官能团为___________和___________(填名称)。
(2)反应⑤中加入试剂X的分子式为C5H4N2Cl2,则X的结构简式为__________________________。
(3)上述①~④反应中,不属于取代反应的是_______________(填序号)。
(4)写出反应①的化学反应方程式___________________________________。
(5)B的一种同分异构体满足下列条件:
Ⅰ能发生很镜反应,能与FeCl3溶液发生显色反应;
Ⅱ分子中有4种不同化学环境的氢原子。
写出一种该同分异构体的结构简式________________________________。
(6)已知:RBr![]() RNH2根据已有知识并结合相关信息,写出以
RNH2根据已有知识并结合相关信息,写出以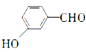 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备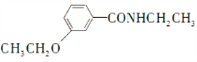 的合成路线流程图(无机试剂任用) ________________________
的合成路线流程图(无机试剂任用) ________________________
合成路线流程图示例如下:
H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com