
【题目】下列对分子性质的解释中,不正确的是
A. 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键
B. 乳酸有一对对映异构体,因为其分子中含有一个手性碳原子
C. 碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”解释
D. 由右图可知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 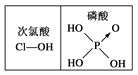
科目:高中化学 来源: 题型:
【题目】下列各选项中,各类物质依次表示为X、Y、Z,其中与图中三个圆所示的从属关系不相符的是:

A. 氧化物、化合物、纯净物
B. 碱性氧化物、金属氧化物、氧化物
C. 胶体、分散系、混合物
D. 复分解反应、置换反应、化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)今有反应2H2+O2===2H2O,要构成燃料电池,则负极通入的应是________,正极通入的应是 ________,电极反应式分别为负极:__________________________、正极:________________。
(2)如把KOH改为稀H2SO4作电解液,则电极反应式分别为负极:__________、正极:______。
(3)如把H2改为甲烷,KOH溶液作电解液,则负极反应式为:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 是三种短周期元素,其中 X、Y 位于同一主族,Y、Z 处于同一周期,X 原子的最外层电子排布式是 2s22p4,Z 原子的核外电子数比 Y 原子少 1。下列说法不正确的是( )
A. CX2(C 是原子核内含 6 个质子的元素)分子是非极性分子
B. ZH3 的 VSEPR 模型名称为三角锥形
C. Z4 分子是非极性分子
D. 酸 H2YO4 比酸 H3ZO4 的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点 A2D<A2X
B. CA3 分子是非极性分子
C. B、C、D 形成的气态氢化物互为等电子体
D. C 形成的常见单质中 σ 键与 π 键个数之比为 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
A. 元素Y、Z、W形成的简单离子具有相同电子层结构,其半径依次增大
B. 元素Y、R分别与元素X形成的化合物的稳定性:XmY强于XmR
C. 元素Z、Y形成的1mol化合物中含有的分子数约为1.806×1024
D. 元素Z、R的最高价氧化物水化物之间相互反应生成的盐溶液呈中性或碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用 VSEPR 理论判断下表中分子或离子的立体构型。
分子 | 中心原子上弧电子对数 | 中心原子结合的杂化类型 | 分子或离子的立体构型 |
NH2 | _______________ | _______________ | _______________ |
BF3 | _______________ | _______________ | _______________ |
H3O+ | _______________ | _______________ | _______________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)如何检验绿矾晶体中Fe2+是否被氧化?_______________________________
(2)已知本实验所用绿矾晶体没有被氧化。为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。

①将下列实验操作步骤正确排序__________(填标号);重复上述操作步骤,直至装置A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量装置A的质量 f.冷却到室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_____________(列式表示)。若实验时按a、d次序操作,则使x_____________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红色粉末。
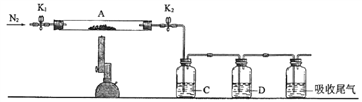
①C、D中的溶液依次为__________(填标号)。C、D中有气泡冒出,并可观察到的现象分别为_____________。
A.品红 B.NaOH C.BaCl2 D.Ba(NO3)2 E.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_______________。
(4)绿矾溶液在空气中久置出现红褐色沉淀,写出相关的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种气体,A是密度最小的气体,B在通常情况下呈黄绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D。把无色无刺激气味气体C通入澄清石灰水时变浑浊。
(1)A、B、C、D的分子式分别为:A_______ B________ C_________D_______。
(2)写出下列各反应的化学方程式:
A与B_______________________________________________;
B与水_______________________________________________;
C与澄清石灰水_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com