
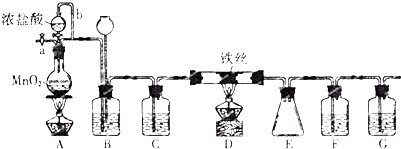
分析 根据实验装置图可知,用浓盐酸与二氧化锰反应生成氯气,氯气中有氯化氢和水杂质,为制备并收集无水FeCl3,B装置中装饱和食盐水,除去氯气中的氯化氢,通过装置中的长颈漏斗可判断实验过程中导管是否被产品堵塞,C装置中装浓硫酸干燥氯气,D装置中铁与氯气反应生成氯化铁,E装置收集生成的氯化铁,实验尾气中有氯气,要用氢氧化钠溶液吸收,由于无水FeCl3极易潮解,所以在收集装置和尾气吸收装置之间加一个干燥装置,防止吸收装置中的水份与氯化铁反应,所以F中装浓硫酸,G中装氢氧化钠溶液,实验时由于装置中有空气中的水蒸气,会与氯化铁反应,所以要先排除装置中的空气,据此答题.
解答 解:根据实验装置图可知,用浓盐酸与二氧化锰反应生成氯气,氯气中有氯化氢和水杂质,为制备并收集无水FeCl3,B装置中装饱和食盐水,除去氯气中的氯化氢,通过装置中的长颈漏斗可判断实验过程中导管是否被产品堵塞,C装置中装浓硫酸干燥氯气,D装置中铁与氯气反应生成氯化铁,E装置收集生成的氯化铁,实验尾气中有氯气,要用氢氧化钠溶液吸收,由于无水FeCl3极易潮解,所以在收集装置和尾气吸收装置之间加一个干燥装置,防止吸收装置中的水份与氯化铁反应,所以F中装浓硫酸,G中装氢氧化钠溶液,实验时由于装置中有空气中的水蒸气,会与氯化铁反应,所以要先排除装置中的空气,
①加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应的离子方程式为:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;
故答案为:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;
②根据上面的分析可知,装置F中所加的试剂为浓硫酸或浓H2SO4,
故答案为:浓硫酸或浓H2SO4;
③根据装置图可知,导管b的作用为平衡压强(或使浓盐酸顺利流下),装置B的作用为除去Cl2中的HCl气体,通过装置中的长颈漏斗可判断实验过程中导管是否被产品堵塞,
故答案为:平衡压强(或使浓盐酸顺利流下);除去Cl2中的HCl气体、判断实验过程中导管是否被产品堵塞;
④根据上面的分析可知,实验时应先排尽实验装置中的空气,所以实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,
故答案为:排尽实验装置中的空气;
⑤为减少氯气对空气的污染,反应结束后,拆卸装置前,必须进行的操作是打开活塞a,通入空气把装置内残留的Cl2排出,保证吸收更彻底(,
故答案为:打开活塞a,通入空气把装置内残留的Cl2排出,保证吸收更彻底.
点评 本题以氯化铁的制备为背景,考查了氯气的制备和性质的检验,解题关键理在于明确实验原理和目的及各装置的作用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该绿色晶体配体是氯离子和水,它们物质的量之比为1:5 | |
| B. | 紫色晶体配合物的化学式为[Ti(H2O)6]Cl3 | |
| C. | 上述两种晶体的分子式相同,但结构不同,所以性质不同 | |
| D. | 0.01mol 紫色晶体在水溶液中与过量AgNO3作用最多可得到 2.78 g 沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 | |
| B. | 热化学方程式各物质前的化学计量数只表示分子个数不代表物质的量 | |
| C. | 燃烧热或中和热是反应热的种类之一 | |
| D. | 对于H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl△H<0,断开1mol H-H键和1mol Cl-Cl键所吸收的总能量大于形成2mol H-Cl键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | -57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
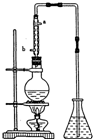
 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
| 密度(g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环已醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环已烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$ n(C2H4O)
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$ n(C2H4O)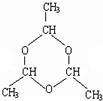 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com