
【题目】实验室中Y形管是一种特殊的仪器,通常与其他仪器组合可以进行某些实验探究。利用下图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。回答下列问题:

(1)广口瓶中间那根玻璃管的作用是:__________________________________________。
(2)实验前需要将BaCl2溶液煮沸,其目的是:_________________________________。
(3)甲中发生反应的化学方程式为:____________________________________________。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体。该反应的化学方程式为:____________________________________________。
(5)实验时,先使甲中产生的足量气体通入BaCl2溶液中,始终无沉淀生成。由此得出的结论是_______。
(6)向上述⑸实验所得溶液中通入乙产生的气体,产生白色沉淀,请写出发生反应的离子方程式:_____。
(7) 请指出该实验的一个不足之处:____________________________________________。
【答案】平衡压强,使甲、乙中的气体可顺利进入BaCl2溶液中 排除溶解的O2防止将SO2在溶液中氧化为SO42-而对实验产生干扰 Na2SO3+H2SO4(浓)=SO2↑+Na2SO4+H2O CaO + NH3·H2O=Ca(OH)2+NH3↑(或NH3·H2O![]() NH3↑ +H2O ) 在酸性条件下不能生成BaSO3沉淀 SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+ SO2可能对环境产生污染(或没尾气处理装置)、通NH3时有可能倒吸
NH3↑ +H2O ) 在酸性条件下不能生成BaSO3沉淀 SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+ SO2可能对环境产生污染(或没尾气处理装置)、通NH3时有可能倒吸
【解析】
本题的实验目的是探究SO2与BaCl2反应生成BaSO3沉淀的条件。甲装置中Na2SO3与浓H2SO4反应制备SO2;为了防止BaCl2溶液中溶解的O2与SO2作用产生的SO42-干扰实验的判断,实验前需要将BaCl2溶液煮沸赶尽溶解氧;通过实验现象得出在酸性条件下SO2不能与BaCl2反应生成BaSO3沉淀;装置乙中产生的碱性气体为NH3,由CaO和氨水作用产生NH3;SO2、NH3通入BaCl2溶液中产生BaSO3沉淀;SO2、NH3都能污染大气,NH3极易溶于水,该装置的不足之处是没有尾气吸收装置、通NH3时可能产生倒吸;根据上述分析作答。
(1)广口瓶中间那根玻璃管的作用是:平衡压强,使甲、乙中的气体可顺利进入BaCl2溶液。
(2)为了防止BaCl2溶液中溶解的O2与SO2作用产生的SO42-干扰实验的判断,实验前需要将BaCl2溶液煮沸,其目的是:排除溶解的O2,防止将SO2在溶液中氧化为SO42-而对实验产生干扰。
(3)甲中Na2SO3与浓H2SO4反应生成Na2SO4、H2O和SO2,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体,该碱性气体为NH3,获得NH3的常用氧化物为CaO、无色液体为氨水,两者反应的化学方程式为:CaO+NH3·H2O=Ca(OH)2+NH3↑。
(5)实验时,将甲中产生的足量SO2通入BaCl2溶液中,始终无沉淀生成,由此说明:酸性条件下SO2不能与BaCl2反应生成BaSO3沉淀。
(6)向上述(5)实验所得溶液中通入NH3,产生白色沉淀,反应的化学方程式为SO2+2NH3+H2O+BaCl2=BaSO3↓+2NH4Cl,反应的离子方程式为SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+。
(7)SO2、NH3都能污染大气,该装置的不足之处是没有尾气吸收装置;NH3极易溶于水,该装置的不足之处是装置中d导管插入BaCl2溶液中,通NH3时可能产生倒吸。


科目:高中化学 来源: 题型:
【题目】硝酸铵能与强碱反应,其中与烧碱反应的方程式: NH4NO3+NaOH===NaNO3+NH3↑+X。其中X物质是
A.COB.O2C.H2OD.O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体的还原性,装置如图所示,下列说法不合理的是
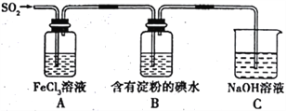
A. A装置中FeCl3溶液逐渐变为浅绿色,可以说明SO2有还原性
B. B装置中蓝色退去,说明还原性:SO2>I-
C. C装置中吸收尾气有可能倒吸
D. A、B装置中发生的反应转移电子数一定相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是![]()
![]()
A. 标准状况下,![]() 氯气与足量水反应,转移电子数目为
氯气与足量水反应,转移电子数目为![]()
B. ![]() 中含有的质子数为
中含有的质子数为![]()
C. 12g金刚石中含有的共价键数为![]()
D. 标准状况下,![]() 氟化氢中含有氟原子的数目大于
氟化氢中含有氟原子的数目大于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源公交、轻轨、云轨等使淮安交通更加快捷。“车联网”技术定位车辆运行轨迹的光纤材料二氧化硅功不可没,二氧化硅属于
A. 分子晶体 B. 离子晶体 C. 原子晶体 D. 金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

![]() 该浓盐酸的物质的量浓度为 ______
该浓盐酸的物质的量浓度为 ______ ![]() .
.
![]() 取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ______ .
取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ______ .
A.溶液中HCl的物质的量![]() 溶液的浓度
溶液的浓度
C.溶液中![]() 的数目
的数目![]() 溶液的密度
溶液的密度
![]() 某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为
某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为![]() 稀盐酸.
稀盐酸.
![]() 该学生需要量取 ______ mL上述浓盐酸进行配制.
该学生需要量取 ______ mL上述浓盐酸进行配制.
![]() 配制时,其正确的操作顺序是
配制时,其正确的操作顺序是![]() 用字母表示,每个字母只能用一次
用字母表示,每个字母只能用一次![]() ______ ;
______ ;
A.用30mL水洗涤烧杯![]() 次,洗涤液均注入容量瓶,振荡
次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水![]() 约
约![]() 的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线![]() 处
处
![]() 在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?![]() 填“偏高”或“偏低”或“无影响”
填“偏高”或“偏低”或“无影响”![]() .
.
I、用量筒量取浓盐酸时俯视观察凹液面 ______
II、用量筒量取浓盐酸后,洗涤量筒![]() 次,洗涤液也转移到容量瓶 ______
次,洗涤液也转移到容量瓶 ______
III、溶液注入容量瓶前没有恢复到室温就进行定容 ______
![]() 若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d
若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d![]() ,则此溶液的物质的量浓度为 ______
,则此溶液的物质的量浓度为 ______ ![]() 填字母
填字母![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如下图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极,下列说法正确的是
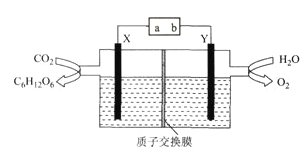
A. 电源a极为正极
B. 该装置中Y电极发生还原反应
C. X电极的电极反应式为6CO2+24H++24e-=C6H12O6+6H2O
D. 理论上,每生成22.4L(标准状况下)O2,必有4mol H+由X极区向Y极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )
A.由同一种元素组成的物质一定是纯净物
B.两种元素只能组成一种化合物
C.一种元素在同一种化合物中只能显示一种价态
D.金属元素在化合物中只显示正化合价,而非金属元素在化合物中可以显示正化合价或负化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,由钴氧化物负载的锰氧化物纳米粒子催化剂对某些反应具有高活性,应用前景良好。回答下列问题:
(1)Mn基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是________;Mn与Co相比,基态原子核外未成对电子数较少的是_______。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)沸点相比较:
①甲醇____H2O(填写“>”“<”或“=”);原因是_____________________________;
②CO2____H2(填写“>”“<”或“=”);原因是________________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了π键外,还存在________。
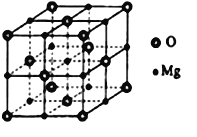
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为αnm,则r(O2-)为________ nm (用含α的算式表示,不必运算化简,下同)。MnO也属于NaCl型结构,晶胞参数为αˊnm,则r(Mn2+)为________nm(用含α、αˊ的算式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com