
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2能使紫色石蕊试液褪色 |
| B | 浓硫酸具有吸水性和强氧化性 | 将浓硫酸滴到用水润湿的蔗糖中,蔗糖变黑色海绵状 |
| C | 在一定条件下铁与水可以发生反应 | 将水蒸气通过灼热的铁粉,粉末变红 |
| D | 盐类水解都是吸热反应 | 向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深。 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.SO2通入品红溶液,溶液褪色的原理与SO2通入溴水后褪色的原理相同 |
| B.浓硫酸具有强氧化性,稀硫酸不具有氧化性 |
| C.用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体 |
| D.明矾和漂白粉常用于自来水的净化和杀菌消毒,但二者的作用原理不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将过量的氯气通入30mL浓度为10.0mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3的共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.15 mol |
| B.当反应中被氧化的氯元素和被还原的氯元素之比为1:4时,溶液中NaClO和NaClO3的物质的量之比为3:1 |
| C.溶液中n(Na+):n(Cl-)可能为7:3 |
| D.若Cl2与NaOH的反应中转移的电子为n mol,则0.15<n<0.35 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
通过实验观察,某气体有下列性质:①有刺激性气味;②可使品红溶液褪色;③溶于水其水溶液可使石蕊试液变红;④通入浓硝酸中有红棕色气体产生;⑤可使溴水褪色。据此推测该气体可能是
| A.HCl | B.NH3 | C.Cl2 | D.SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某硫酸厂废气厂SO2的回收利用方案如下图所示,下列说法不正确的是: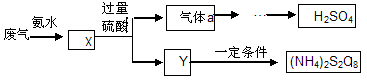
| A.X可能含有2种盐 | B.a是SO3 |
| C.Y可能含(NH4)2SO4 | D.(NH4)2S2O8中S元素的化合价不可能为+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D、E都是中学化学中常见物质,它们均含有同一种短周期元素,在一定条件下可发生如图所示的转化,其中A是单质,B在常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。下列判断中不合理的是( )
A.A不可能是金属 B.由C生成D肯定发生了电子转移
C.由A生成C肯定属于离子反应 D. B与E可能反应生成盐
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三硫化四磷用于制造火柴及火柴盒摩擦面,分子结构如下图所示。下列有关三硫化四磷说法中正确的是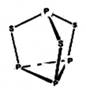
| A.该物质中磷元素的化合价为+3 |
B.该物质分子中含有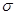 键和 键和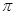 键 键 |
| C.该物质的熔、沸点比食盐高 |
| D.该物质22g含硫原子的数目约为1.806×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O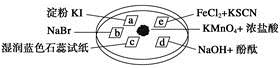
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com