
分析 ①Fe和稀盐酸反应生成氯化亚铁和氢气,所以有大量气泡生成,底部黑色粉末是铁粉;
②难溶性固体和溶液采用过滤方法分离;根据过滤操作所需仪器选取仪器;
③该反应中氧化产物是铁离子,根据铁离子和氯气之间的关系式计算消耗氯气体积;
④铜和氯化铁反应生成氯化亚铁和铜离子.
解答 解:①Fe和稀盐酸反应生成氯化亚铁和氢气,所以有大量气泡生成,底部黑色粉末是铁粉,离子方程式为Fe+2H+=Fe2++H2↑,
故答案为:Fe+2H+=Fe2++H2↑;
②难溶性固体和溶液采用过滤方法分离,氯化亚铁易溶于水,C不易溶于水,所以分离氯化亚铁和碳采用过滤方法;过滤操作用到的玻璃仪器有烧杯、玻璃棒、漏斗,
故答案为:过滤;烧杯、玻璃棒和漏斗;
③该反应中氧化产物是铁离子,设消耗氯气体积为V,
2Fe2++Cl2=2Fe3++2Cl─;
22.4L 112g
V ag
22:4L:112g=V:ag
V=$\frac{22.4L×ag}{112g}$=0.2aL,
故答案为:0.2a;
④铜和氯化铁反应生成氯化亚铁和铜离子,离子方程式为 2Fe3++Cu=Cu2++2Fe2+,
故答案为:2Fe3++Cu=Cu2++2Fe2+.
点评 本题考查离子方程式书写、化学方程式计算、物质分离提纯等知识点,侧重考查学生分析判断计算能力,明确元素化合物性质、各物质之间的关系水解本题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
A.Na2CO3是碱 B.Na2CO3是盐 C.Na2CO3是钠盐 D.Na2CO3是碳酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
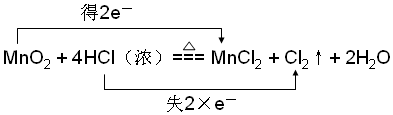 .
.查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒承接,该溶液的体积应为
A.10mL B.40mL C.大于40mL D.小于40mL
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
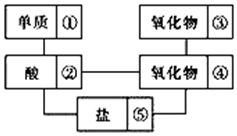 在稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉9种物质间存在下面的相互关系,选择①-⑤中适当的物质,使有连线的两种物质能发生反应.
在稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉9种物质间存在下面的相互关系,选择①-⑤中适当的物质,使有连线的两种物质能发生反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s22s22p63s23p63d104s1 | B. | 1s22s22p63s23p63d64s2 | ||
| C. | 1s22s22p63s23p63d34s2 | D. | 1s22s22p63s23p63d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4→HCl→K2S→NaOH→CO2 | B. | NaCl→Na2SO4→Na2S→NH3•H2O→HCl | ||
| C. | Na2S→Na2SO4→NaCl→NaOH→HCl | D. | NaCl→Na2SO4→H2S→NaOH→CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相等 | B. | 后者是前者的11倍 | ||
| C. | 后者是前者的108 | D. | 前者是后者的108 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
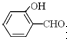 形成分子内氢键,而
形成分子内氢键,而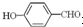 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com