
【题目】积极保护生态环境可实现人与自然的和谐共处.
①下列做法会加剧温室效应的是(填字母).
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是(填字母).
a.使用可降解塑料 b.露天焚烧废弃塑料 c.直接填埋废弃塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹.“禁止燃放烟花爆竹”的标识是(填字母).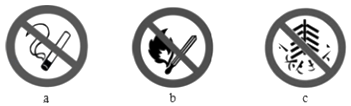
【答案】b;a;c
【解析】解:①a.植树造林 能够控制二氧化碳的含量升高,有利于减缓温室效应,故不选;
b.燃煤供暖,煤燃烧能够生成二氧化碳,燃烧时会导致温室效应加剧,故选;
c.风力发电属于清洁能源,不会放出二氧化碳,有利于减缓温室效应,故不选;
故选b;
②a.使用可降解塑料可以减少塑料制品的使用,能够防治“白色污染”,故选;
b.露天焚烧废弃塑料会产生大量的有害气体,污染空气,不能够防治“白色污染”,故不选;
c.废弃塑料难降解,将废弃塑料直接填埋,埋会占用较大空间,塑料自然降解需要百年以上,析出添加剂污染土壤和地下水,会引起白色污染,故不选;
故选a;
③根据烟花爆竹的图案,则“禁止燃放烟花爆竹”的标识是c,
故选:c.


科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此推断错误的是
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此推断错误的是

A. 正反应是放热反应
B. A、B一定都是气体
C. D一定不是气体
D. C可能是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》曾记载利尿剂甘汞(Hg2Cl2)制法:"用水银一两,白矾[KAl(SO4)2]二两,食盐一两,同研,不见星。铺于器内,以小乌盆覆之,筛灶灰,盐水和,封固盘口,以炭打二柱香取开,则粉升于盆上矣,其白如雪,轻盈可爱,一两汞可升粉八钱。”
(1)甘汞(Hg2Cl2)中化学键类型主要为___________.
(2)[KAl(SO4)2]所属物质类别为__________ (填标号)
A.酸式盐 B.复盐 C.正盐 D.混盐 E.硫酸盐
(3)文中“同研”涉及的操作,若在实验室通风橱内完成,则所需的仪器是_______。
(4)文中“则粉升于盆上矣”涉及的混合物分离方法是__________
(5)甘汞(Hg2Cl2)制备反应中,氧化剂与还原剂的物质的量之比为_________,该反应中还原产物是__________。
(6)已知文中一两等于十钱,则甘汞的产率约为________(保留三位有效数字)。
(7)由甘汞(Hg2Cl2)光照可得外科用药升汞(HgCl2),该反应化学方程式为___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子的原子核外有三个电子层,K层电子数为a,L层电子数为b,M层电子数为b-a,该原子核内的质子数是(
A. 14 B. 15 C. 16 D. 17
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的 CrO72﹣和 CrO42﹣ , 它们会对生态系统产生很大的伤害,工业上对废水处理的工艺流程如下:CrO42﹣ ![]() Cr2O72﹣→
Cr2O72﹣→ ![]() Cr3+→
Cr3+→ ![]() Cr(OH)3↓
Cr(OH)3↓
(1)CrO42﹣中 Cr 的化合价;Cr3+的核外电子排布式为 .
(2)写出第①步发生的离子反应方程式;若常温下,减 小平衡体系的 pH 至 pH=2,则溶液趋向于显色(.
(3)第②步中,还原 0.01mol Cr2O72﹣离子,需要mol 的 FeSO47H2O.
(4)已知 Cr(OH)3 在溶液中存在以下平衡:H++CrO2﹣+H2OCr(OH)3Cr3++3OH
下列有关说法中正确的是
a.加 HCl 则平衡均向右移动,则生成 Cr3+盐
b.按照物质分类 Cr(OH)3是两性氢氧化物,属于弱电解质
c.Cr3+盐中逐滴加入 NaOH 溶液,先产生沉淀,后沉淀消失
d.Cr(OH)3 饱和溶液中一定有 c(H+ )=c(OH﹣ )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是( )
A. Na、Mg、Al原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F第一电离能依次增大
D. Na、K、Rb电负性逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能说明X的电负性比Y大的是 ( )
A. 与氢化合时X单质比Y单质容易
B. X的最高价氧化物对应水化物的酸性比Y的强
C. X原子的最外层电子数比Y原子的最外层电子数多
D. X的单质可以把Y从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是 ( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F电负性依次增大
D. Na、K、Rb第一电离能逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锰(MnCO3)是高性能磁性材料,金属钨是重要的战略物资。由黑钨矿(主要成分为FeWO4、MnWO4,少量SiO2)制取碳酸锰和金属钨的流程如下:

已知:①钨酸(H2WO4)酸性很弱,难溶于水,其钠盐易溶于水。②SiO32-和WO42-完全沉淀的pH分别为8、5。③草酸(H2C2O4)具有酸性和还原性,能分解。
回答下列问题:
(1)将矿石粉碎的目的是_____________________。
(2)固体(X)的化学式是____________________________。
(3)写出高温焙烧过程中,MnWO4发生反应的化学方程式________________。
(4)MnO2与硫酸、草酸反应的离子方程式是__________________________。测得一定量MnO2完全溶解的时间与温度的关系如图所示,分析控温加热75℃时MnO2溶解所需时间最少的原因__________________。

(5)滤液Ⅱ调节pH应选择的试剂为_________________。
A.WO3 B.氨水 C.稀盐酸 D.NaHCO3
(6)用Na2CO3溶液沉淀Mn2+时,应控制MnSO4溶液的pH不超过8,防止生成Mn(OH)2,用Na2CO3溶液沉锰采取的操作方法是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com