
【题目】下列实验过程中沉淀的物质的量(Y)与加入的试剂的量(X)之间的关系正确的是( )
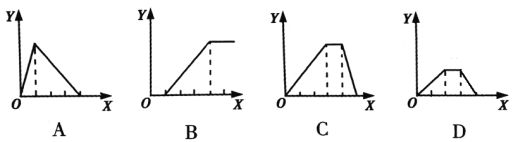
A.如图A:向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡
B.如图B:向NaAlO2溶液中滴加盐酸且边滴边振荡
C.如图C:向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量
D.如图D:向等物质的量的NaOH、Ba(OH)2的混合溶液中逐渐通入二氧化碳至过量
【答案】C
【解析】
A.向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡,先产生氢氧化铝沉淀:AlCl3+3NaOH=Al(OH)3↓+3NaCl,继续滴加NaOH溶液,Al(OH)3和NaOH溶液反应,生成偏铝酸钠,沉淀溶解:NaOH+Al(OH)3=NaAlO2+2H2O,所以沉淀量达到最大消耗NaOH和沉淀溶解消耗NaOH的比为3:1,故A错误;
B.向NaAlO2溶液中滴加稀盐酸,立刻产生白色氢氧化铝沉淀,发生反应:AlO2-+H++H2O=Al(OH)3↓,随着盐酸的逐滴加入,开始形成的沉淀又逐渐溶解,发生反应:Al(OH)3+3H+=Al3++3H2O,所以沉淀量达到最大消耗的盐酸和沉淀完全溶解消耗的盐酸的物质的量之比是1:3,故B错误;
C.向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液,开始滴加NaOH发生反应为Al3++3OH-=Al(OH)3↓,先产生氢氧化铝沉淀,当Al3+沉淀完全后,然后发生反应NH4++OH-=NH3H2O;此时沉淀氢氧化铝的量不变,最后继续滴加NaOH,发生反应Al(OH)3+OH-=AlO2-+2H2O,氢氧化铝沉淀溶解,沉淀量达到最大消耗NaOH、沉淀量不变和沉淀溶解消耗NaOH的比为3:1:1,故C正确;
D.向等物质的量的NaOH、Ba(OH)2的混合溶液中逐渐通入二氧化碳至过量,首先发生反应:Ba(OH)2+CO2=BaCO3↓+H2O,产生白色沉淀,然后发生:CO2+2NaOH=Na2CO3+H2O,此时沉淀的量不变,又发生反应:Na2CO3+H2O+CO2=2NaHCO3,沉淀量不变,最后发生反应:BaCO3+2H2O+2CO2=Ba(HCO3)2,沉淀部分溶解,沉淀量达到最大消耗CO2、沉淀量不变和沉淀溶解消耗CO2的比为1:2:2,故D错误;
答案选C。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组模拟上述过程,所设计的装置如图所示:
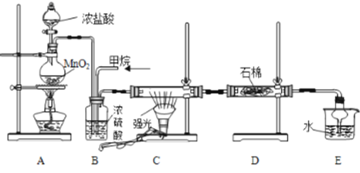
(1)A中制取Cl2时若将MnO2换成另一种固体即可不用加热并能快速制取氯气,写出该快速制氯气过程的离子方程式为______。
(2)B装置有三种功能:①控制气流速度;②___________;③___________。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是___________。
(4)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是___________。
(5)该装置还存在的明显缺陷是____________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(9分) 观察下列几个装置示意图,有关叙述正确的是
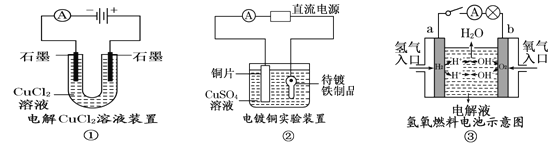
(1)在①图中,发生反应的化学方程式为: 。
(2)在②图中,待镀铁制品应与电源 极相连,电极反应式为: 。
(3)在③图中,外电路电子由 极流向 极,若电解液为KOH溶液,则b极的反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证还原性:SO2>Fe2+>C1-,三组同学分别进行了下图实验,并对溶液1和溶液2中所含离子进行了检验,能证明上述还原性顺序的实验组有
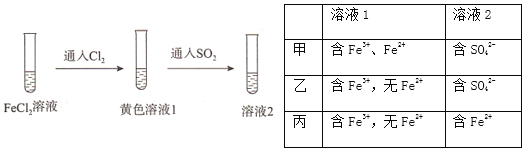
A. 只有甲 B. 甲、乙 C. 甲、丙 D. 甲、乙、丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某石油化工产品X的转化关系如图,下列判断不正确的是( )
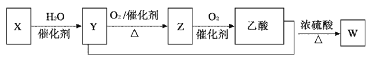
A. X可以发生加聚反应B. Y能与钠反应产生氢气
C. Z与CH3OCH3互为同分异构体D. W的结构简式为CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用核磁共振技术测定有机物分子的三维结构的研究曾获得诺贝尔化学奖。在有机物分子中,不同位置的氢原子的核磁共振氢谱中给出的峰值(信号)也不同。根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
例如:乙醚的结构式为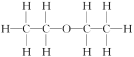 ,其核磁共振氢谱中有2个峰(信号)(参见下图)。
,其核磁共振氢谱中有2个峰(信号)(参见下图)。
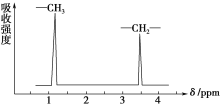
CH3CH2OCH2CH3的核磁共振氢谱
(1)下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是________。
A.CH3CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
(2)化合物A和B的分子式都是C2H4Br,A的核磁共振氢谱如图所示,则A的结构简式为________,请预测B的核磁共振氢谱上有________个峰(信号)。
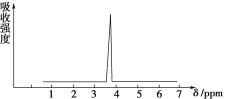
A的核磁共振氢谱示意图
(3)用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂采用如图装置处理化石燃料开采、加工过程产生的H2S废气,已知电解池中的两个电极均为惰性电极。下列说法不正确的是
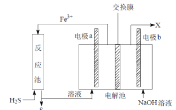
A.若交换膜为质子交换膜,则NaOH溶液的浓度逐渐变大,需要定期更换
B.若交换膜为阳离子交换膜,b 电极区会产生红褐色沉淀
C.电极 a 为阳极
D.反应池中处理H2S的反应是H2S +2Fe3+ = 2Fe2+ +S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应方程式不正确的是
A.用Cl2与石灰制取漂白粉:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
B.工业上用焦碳与石英砂制粗硅:SiO2+C![]() Si+CO2
Si+CO2
C.高温下铁与水蒸汽反应:3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
D.小苏打溶液与少量石灰水反应:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅孔雀石[主要成分为 CuCO3Cu(OH)2、CuSiO32H2O,含 SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如下:
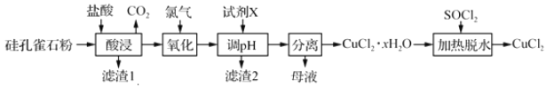
已知:SOCl2+H2O ![]() SO2↑+2HCl↑
SO2↑+2HCl↑
(1)“酸浸”时盐酸与CuCO3Cu(OH)2反应的化学方程式为________________,为提高“酸浸”时铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③_________;
(2)滤渣2的主要成分为___________(填化学式);
(3)“氧化”时发生反应的离子方程式为__________________________;
(4)试剂X的作用是调节溶液的pH,试剂X可以是_____;“调pH”时,pH不能过高,其原因是_______________;
A.CuSO4 B.Cu2(OH)2CO3 C.NaOH D.CuO
(5)“加热脱水”时,加入SOCl2的目的是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com