
下列离子方程式正确的是
A.过量氯气通入溴化亚铁溶液中2Fe2++2Br-+2Cl2====Fe3++Br2+4Cl-
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C.碳酸氢钙和过量的氢氧化钠溶液反应:Ca2++ OH—+HCO3—=CaCO3↓+ H2O
D.用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Fe2++Cu2+
科目:高中化学 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:填空题
(7分)某消毒液的主要成分为 NaClO(混有少量 NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH溶液吸收 Cl2 制备,化学方程式为__________。
(2)该消毒液的 pH 约为 12,离子方程式为________________。
(3)向 FeSO4 溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为_______________。
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生 1 mol Cl2,转移电子个数约为_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省白城市高一上第一次月考化学试卷(解析版) 题型:选择题
A、B、C、D可能是Na2CO3、HCl、AgNO3、BaCl2四种无色溶液中的某一种,把它们两两混合后产生的现象如下表,则A、B、C、D四种物质按顺序排列正确的是
反应物 | A+B | A+C | B+C | C+D | B+D |
现象 | 白↓ | 白↓ | 白↓ | 白↓ | 无色↑ |
A.BaCl2、 Na2CO3、 AgNO3、 HCl
B.Na2CO3、 HCl、 AgNO3、 BaCl2
C.HCl、 AgNO3、 Na2CO3、 BaCl2
D.AgNO3、 Na2CO3、 BaCl2、 HCl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷(解析版) 题型:选择题
在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g) 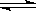 xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
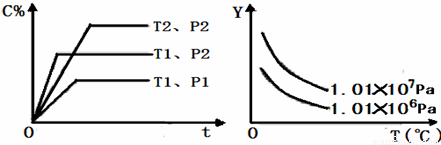
A.反应物A的百分含量 B.平衡混合气中物质B的百分含量
C.平衡混合气的密度 D.平衡混合气的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷(解析版) 题型:选择题
在容积为2升的密闭容器中,有反应:mA(g)+nB(g) 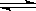 pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=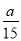 mol·L-1·min-1,C增加了
mol·L-1·min-1,C增加了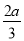 mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为
mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为
A.1︰1︰1︰1 B.1︰3︰2︰2
C.1︰3︰2︰1 D.3︰1︰2︰2
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ·mol-1
②NO2-(aq)+1/2O2(g)=NO3-(aq) △H=-73kJ·mol-1
下列说法正确的是( )
A.1mol的NH3和1mol的NH4+都有10×6.02 ×1023个质子
B.室温下,NH4NO2溶液呈酸性,则说明Ka(HNO2)< Kb(NH3·H2O)
C.NH4+(aq)+2O2(g) NO3—(aq)+2H+(aq)+H2O(l);△H= - 346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
将15.6 g Na2O2和5.4 g Al同时放入一定量的水中,充分反应后得到200 mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则下列说法正确的是
A.标准状况下,反应过程中得到6.72 L气体
B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最终得到7.8 g沉淀
D.最终得到的溶液中c(Na+)=1.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届全国推荐高三联考(二)化学试卷(解析版) 题型:填空题
(12分) 软锰矿(主要成分MnO2,含Fe,Al2O3 ,MgO杂质)的水悬浊液与烟气中的SO2反应可制备MnSO4·H2O,MnO2与SO2反应的化学方程式为MnO2 +SO2=MnSO4。已知下列信息:
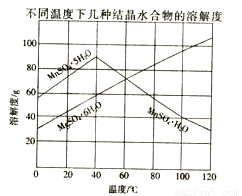
室温下几种氢氧化物的溶度积

回答下列问题:
(1)质量为17.40 g纯净MnO2最多能氧化 L(标准状况) SO2。
(2)悬浊液吸收烟气后,Fe首先转化为Fe2+进入溶液,然后被 氧化为Fe3+;要证明溶液中存在Fe3+,可选择的试剂是 (填标号)。
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室温下,将吸收液过滤,在滤液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是 。
(4)从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③苯酚钠溶液和CO2
④硝酸银溶液和氨水 ⑤氯化铝溶液和氨水 ⑥碳酸氢钠溶液与澄清石灰水
A.③⑤ B.①③⑥ C.仅有⑤ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com