
【题目】实验室制取Cl2及性质的验证实验组合装置如下,请回答下列问题:
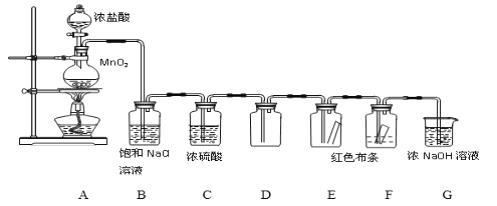
(1)图中装浓盐酸的玻璃仪器名称是________________,
(2)A中发生的离子方程式为____________________________________,若产生的氯气标准状况下为5.6L,参加反应的二氧化锰为_______克。
(3)装置D采用向上排空气收集氯气的原因是_______________________。
(4)能证明干燥的氯气没有漂白性的现象是________________________。
(5)B的作用是____________,G中的化学方程式为________________________。
【答案】分液漏斗 4H+ + 2Cl-+ MnO2 ![]() Mn2+ + Cl2↑+ 2H2O 21.75 氯气密度比空气大 E中红色布条不褪色、F中红色布条褪色 除去HCl气体 Cl2 + 2NaOH = NaCl + NaClO + H2O
Mn2+ + Cl2↑+ 2H2O 21.75 氯气密度比空气大 E中红色布条不褪色、F中红色布条褪色 除去HCl气体 Cl2 + 2NaOH = NaCl + NaClO + H2O
【解析】
(1)装浓盐酸的玻璃仪器名称是分液漏斗;
(2)浓盐酸和二氧化锰反应生成氯化锰、氯气和水,根据化学方程式中物质的量之比等于化学计量数之比进行计算;
(3)氯气密度比空气大,采用向上排空气法收集;
(4)氯气遇到干燥的有色布条不能褪色,起漂白作用的是次氯酸;
(5)饱和NaCl溶液的作用是除去Cl2中的HCl气体,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水。
(1)依据仪器形状可知,装浓盐酸的玻璃仪器名称是分液漏斗,故答案为:分液漏斗。
(2)在加热条件下,实验室可用浓盐酸和二氧化锰制取氯气,二者反应生成氯化锰、氯气和水,离子反应方程式为:4H+ +2Cl-+MnO2![]() Mn2++Cl2↑+2H2O;5.6LCl2的物质的量为5.6L÷22.4L/mol=0.25mol,由反应方程式可知:MnO2~Cl2↑,所以生成0.25molCl2,参加反应的二氧化锰为0.25mol,质量为0.25mol×87g/mol=21.75g,故答案为:4H+ +2Cl-+MnO2
Mn2++Cl2↑+2H2O;5.6LCl2的物质的量为5.6L÷22.4L/mol=0.25mol,由反应方程式可知:MnO2~Cl2↑,所以生成0.25molCl2,参加反应的二氧化锰为0.25mol,质量为0.25mol×87g/mol=21.75g,故答案为:4H+ +2Cl-+MnO2![]() Mn2++Cl2↑+2H2O,21.75。
Mn2++Cl2↑+2H2O,21.75。
(3)装置D采用向上排空气收集氯气的原因是氯气密度比空气大,故答案为:氯气密度比空气大。
(4)氯气遇到干燥的红色布条不能褪色,起漂白作用的是次氯酸,因为干燥氯气不能使干燥的红色布条褪色无漂白性,而氯气能使湿润的红色布条褪色,是因为氯气和水反应生成了次氯酸,次氯酸具有漂白性,故答案为:E中红色布条不褪色、F中红色布条褪色。
(5)饱和NaCl溶液的作用是除去Cl2中的HCl气体,氯气是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收,反应方程式为:Cl2+2NaOH=NaCl +NaClO+H2O,故答案为:除去HCl气体,Cl2+2NaOH=NaCl+NaClO+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】列有机化合物中都含有多个官能团:
A.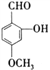 B.
B.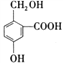 C.
C.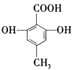 D.
D.![]() E.
E.![]()
(1)可以看作醇类的是________.
(2)可以看作酚类的是________.
(3)可以看作羧酸类的是________.
(4)可以看作酯类的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示法正确的是( )
A. 等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B. 由C(石墨)→C(金刚石)ΔH=+1.9 kJ·![]() 可知,金刚石比石墨稳定
可知,金刚石比石墨稳定
C. 在稀溶液中:H+(aq)+OH﹣(aq)====H2O(l) ΔH=﹣57.3 kJ·![]() ,若将含1 mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
,若将含1 mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
D. 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l)ΔH=+285.8 kJ·![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏加德罗常数和气体摩尔体积等的说法正确的是 ( )
A. 标准状况下,1摩尔SO3的体积约为22.4L
B. 92克NO2气体在标准状况下的体积约为44.8L
C. 同温同压下两种气体的体积之比等于摩尔质量之比
D. 标准状况下,22.4L O2所含的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)取3.7g某有机物A在足量氧气中充分燃烧,只生成8.8 gCO2和4.5g H2O,则A中含有的元素为_________________(填元素符号),其实验式为____________。
(2)下图是A的质谱图,则其相对分子质量为 ________ ;分子式为 _________;
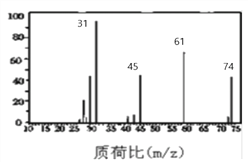
(3)经测定,A在核磁共振氢谱中出现四个峰,吸收峰面积之比为6:1:2:1;A与金属钠反应产生氢气;则A的结构简式为 ____________________________。
(4)A有多种同分异构体,写出与A具有相同官能团的同分异构体的结构简式(任写两种):_________________________,_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为检验木炭和浓硫酸反应生成的产物,设计如图装置(已知SO2能使溴水褪色),请回答:
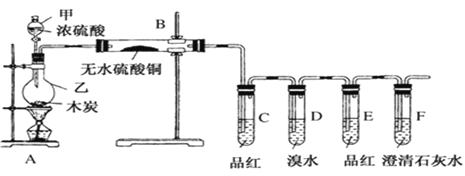
(1)试管D中发生反应的化学方程式为______________________;
(2)试管B中现象是_________________________;
(3)F试管中澄清石灰水的作用是__________________________;
(二)同时该小组设计如下图所示的实验装置(固定装置略),进行SO2性质的研究:
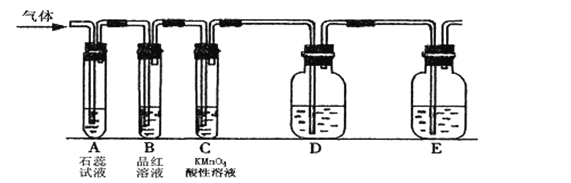
(4)当通入SO2时,A中紫色石蕊溶液变红,用化学方程式解释其原因是___________。
(5)可用来验证SO2具有漂白性的现象是:_______________________。
(6)从元素化合价的角度分析,SO2的性质:
①当通入SO2一段时间后,可观察C中溶液褪色,说明SO2具有_____________性。
②如要验证SO2还具有另一方面的性质,D装置中的药品应为_____________。
A.FeCl3溶液B.氯水C.氢硫酸D.浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.CH3OCH3和CH3CH2OH互为同分异构体B.石墨和C60互为同素异形体
C.35Cl2和37Cl2互为同位素D.C2H6和C4H10互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是( )

①Na、Na2O、Na2O2 ②AlCl3、Al(OH)3、NaAlO2 ③Fe、FeCl2、FeCl3 ④NaOH、Na2CO3、NaHCO3 ⑤C、CO、CO2
A. ①②③④⑤ B. ②④ C. ①③⑤ D. ①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A. 1mol 羟基与1mol 氢氧根离子所含质子数均为9NA
B. 3H2(g)+N2(g) ![]() 2NH3(g) ΔH=-92 kJ/mol,放出热量9.2kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2kJ时,转移电子0.6 NA
C. 5NH4NO3![]() 2HNO3+4N2↑+9H2O 反应中,生成28g N2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O 反应中,生成28g N2,转移的电子数目为3.75NA
D. 密闭容器中2molNO 与1molO2充分反应,产物的分子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com