
【题目】古代炼铜,主要矿物原料是孔雀石 [Cu2(OH)2CO3],燃料是木炭,涉及的反应有:
①Cu2(OH)2CO3 ![]() 2CuO+CO2↑+H2O②2CuO+C
2CuO+CO2↑+H2O②2CuO+C ![]() 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO ![]() Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C ![]() 2CO
2CO
(1)从四种基本反应类型看:反应①、②、④分别属于:______、________、____________。
(2)在上述反应中,属于氧化还原反应的是 __________________(填序号)。其中这几个反应的氧化剂分别是:____________、___________、______________。
【答案】分解反应 置换反应 化合反应 ②③④ CuO CuO CO2
【解析】
(1)根据四种基本反应类型(化合反应、分解反应、复分解反应、置换反应)的特点分析判断;
(2)根据氧化还原反应前后有化合价变化的特征分析判断,结合化合价的变化分析判断。
(1)Cu2(OH)2CO3 ![]() 2CuO+CO2↑+H2O属于分解反应;②2CuO+C
2CuO+CO2↑+H2O属于分解反应;②2CuO+C![]() 2Cu+CO2↑属于置换反应;④CO2+C
2Cu+CO2↑属于置换反应;④CO2+C ![]() 2CO属于化合反应,故答案为:分解反应;置换反应;化合反应;
2CO属于化合反应,故答案为:分解反应;置换反应;化合反应;
(2)①Cu2(OH)2CO3 ![]() 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C ![]() 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO ![]() Cu+CO2;④CO2+C
Cu+CO2;④CO2+C ![]() 2CO四个反应中②③④,反应前后有化合价变化,所以是氧化还原反应;②2CuO+C
2CO四个反应中②③④,反应前后有化合价变化,所以是氧化还原反应;②2CuO+C ![]() 2Cu+CO2↑中CuO中Cu元素的化合价降低,CuO是氧化剂;③CuO+CO
2Cu+CO2↑中CuO中Cu元素的化合价降低,CuO是氧化剂;③CuO+CO ![]() Cu+CO2中CuO中Cu元素的化合价降低,CuO是氧化剂;④CO2+C
Cu+CO2中CuO中Cu元素的化合价降低,CuO是氧化剂;④CO2+C ![]() 2CO中CO2中C元素的化合价降低,CO2是氧化剂,故答案为:②③④;CuO;CuO;CO2。
2CO中CO2中C元素的化合价降低,CO2是氧化剂,故答案为:②③④;CuO;CuO;CO2。


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次递增,X是周期表中非金属最强的元素,W与X同主族,Y、Z是同周期相邻的两种元素,Z元素原子最外层电子数等于周期序数。下列说法正确的是
A.原子半径的大小顺序;![]()
B.简单氢化物的热稳定性:![]()
C.最高价氧化物对应水化物的碱性:![]()
D.工业上,常用电解含Y或Z简单离子溶液的方法冶炼单质Y或Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其中D与A、B、C均能形成原子个数比为1∶1与1∶2的两类化合物X、Y,E的某种含氧酸或含氧酸盐在一定条件下可分解生成D的单质。
(1)由上述条件可以确定的元素编号及对应元素名称是____________,其中原子间通过共用一对电子而形成的单质的电子式为________________,E能形成多种含氧酸,其中酸性最强的含氧酸的分子式为______________。
(2)若所有可能的X、Y中,C、D形成的是离子化合物,其中一种物质中含有两类化学键,那么另一种物质的形成过程用电子式可表示为______________________________________。
(3)若上述X、Y存在如下变化:X+Y→Z+D2,且X、Y中各原子(离子)最外层上均有8个电子,则该反应的化学方程式为__________________,反应物中存在非极性键的物质是__________,生成物中存在非极性键的物质是_____________,由此说明化学反应的本质是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块擦去氧化膜的铝片放入20 mL 0.5 mol·L-1 CuSO4溶液中,观察实验现象。下列方程式不正确的是
A.Cu2+(aq)+2H2O(l)Cu(OH)2(s)+2H+(aq) △H>0
B.2Al(s)+3Cu2+(aq)=2Al3+(aq)+3Cu(s) △H<0
C.Cu(OH)2(s)![]() CuO(s)+H2O(l) △H>0
CuO(s)+H2O(l) △H>0
D.2Al(s)+6H+(aq)=2Al3+(aq)+3H2(g) △H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1000 mol·L-1 NaOH溶液分别滴定0.1000 mol·L-1 HA~HD酸的滴定曲线如图所示。下列说法不正确的是
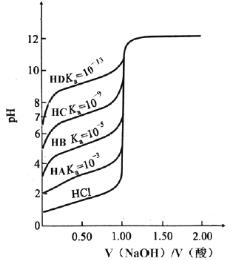
A.等物质的量浓度时,Ka越小滴定突变越不明显,滴定误差越大
B.滴定HC时,滴定终点的pH=7
C.滴定HB时,应该选择酚酞作为指示剂
D.由图像可知在计算HD滴定前溶液pH时不能忽略水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较金属性的强弱:Na_________K(填“>”、“<”或“=”);反应Na+KClNaCl+K↑能发生的原因是________________。
(2)COCl2是共价化合物,各原子均满足8电子稳定结构。写出COCl2的结构式__________。
(3)电解熔融氧化铝制备金属铝时,需要定期更换阳极石墨块,理由是_________________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳在冶金工业上具有重要用途。已知氧与碳的反应主要有:
Ⅰ.C(s)+O2(g)CO2(g) △H1=-394kJ·mol-1
Ⅱ.2C(s)+O2(g)2CO(g) △H2=-221kJ·mol-1
Ⅲ.2CO(g)+O2(g)2CO2(g) △H3
上述反应的△G~T如图所示,且满足△G=△H-T△S。
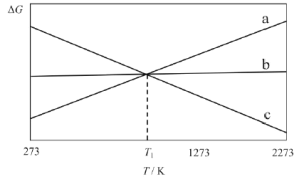
请回答:
(1)曲线a代表反应_________(填“I”、“II”或“III”),理由是__________。
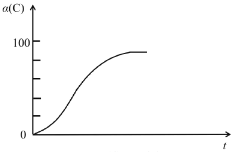
(2)研究发现,以CO2替代高温水蒸气作为煤气化反应(H2O与C反应)的气化剂,实现了CO2零排放的新工艺。写出反应IV的热化学方程式___________(碳的计量数为1)。在1273K时,测得碳转化率[α(C)]与时间t变化如图所示。保持其它条件不变,请画出1773K时α(C)~t关系图______。
(3)当T=T1时,反应IV处于平衡状态,下列关于反应IV的说法正确的是_________。
A.因平衡时△G=0,若△H变化173.3kJ·mol-1,△S变化173.3J·K-1·mol-1,计算得T1=1000K
B.T<T1时,反应向逆反应方向移动
C.当碳的浓度不再变化时,一定处于平衡状态
D.因平衡常数K的值不再变化,反应达到了平衡
(4)当T=1273K时,仅存在CO、CO2两种气体,且维持总压为1 atm,此时反应IV的Kp=112,则CO气体所占的分压p(CO)为___________atm。(列式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)![]() CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是

A. 该反应的△H<0,且p1<p2
B. 反应速率:ν逆(状态A)>ν逆(状态B)
C. 在C点时,CO转化率为75%
D. 在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com