
(16分)(I)某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4 ==H2↑+CuSO4,试回答:
==H2↑+CuSO4,试回答:

(1)该装置的名称是 (填“电解池”或“原电池”)。
(2)A、B中至少有一种是金属 (填名称),接电源的 (填“正极”或“负极”)。
(3)写出该装置中发生还原反应的电极反应方程式为 。
(4)若C溶液为100ml饱和食盐水,A 和B电极均为碳棒,该学生利用图示装置进行电解,写出该电解过程中的总反应的离子方程式 ,当放出标况下112ml氢气时,该溶液的PH= (室温下)。
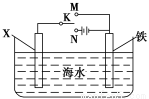
(II)利用下图装置,可以模拟铁的电化学防护。若X为铜,为减缓铁的腐蚀,开关K应置于________处。若X为锌棒,开关K置于M处,该电化学防护法称为 。
(I)(1)电解池 (2)铜 正极 (3)2H+ + 2e- = H2↑
(4)2Cl-+2H2O H2↑+Cl2↑+2OH- 12 (II)N 牺牲阳极阴极保护法
H2↑+Cl2↑+2OH- 12 (II)N 牺牲阳极阴极保护法
【解析】
试题解析:(I) (1)Cu+H2SO4 ==H2↑+CuSO4为非自发的氧化还原反应,需强制实现,故该装置的名称是电解池;(2)该电解池的阳极反应时铜被氧化,故A、B中至少有一种是金属铜,且做电解池的阳极,接电源的正极;(3该装置中氢离子在阴极上发生还原反应,电极反应式为:2H++2e-=H2↑;(4)碳电极电解饱和食盐水时,阳极上氯离子被氧化,阴极上氢离子被还原,总反应的离子方程式为:2Cl-+2H2O
==H2↑+CuSO4为非自发的氧化还原反应,需强制实现,故该装置的名称是电解池;(2)该电解池的阳极反应时铜被氧化,故A、B中至少有一种是金属铜,且做电解池的阳极,接电源的正极;(3该装置中氢离子在阴极上发生还原反应,电极反应式为:2H++2e-=H2↑;(4)碳电极电解饱和食盐水时,阳极上氯离子被氧化,阴极上氢离子被还原,总反应的离子方程式为:2Cl-+2H2O H2↑+Cl2↑+2OH-;当放出标况下112ml氢气时,溶液中生成10-2mol/L的氢氧根,故PH=-lg
H2↑+Cl2↑+2OH-;当放出标况下112ml氢气时,溶液中生成10-2mol/L的氢氧根,故PH=-lg =12;(II)铁比铜活泼性强,若要保护铁,需用外接电源的阴极保护法,铁做阴极,K应置于N处;X为锌比铁活泼,开关K置于M处,形成原电池,用牺牲阳极的阴极保护法保护铁。
=12;(II)铁比铜活泼性强,若要保护铁,需用外接电源的阴极保护法,铁做阴极,K应置于N处;X为锌比铁活泼,开关K置于M处,形成原电池,用牺牲阳极的阴极保护法保护铁。
考点:金属的电化学腐蚀和防护


科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
下列各组性质的比较中正确的是
A.酸性 HClO4<HBrO4<HIO4B.碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2
C.稳定性 HCl>PH3>H2SD.还原性 Cl->Br->I-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高一上学期联考化学试卷(解析版) 题型:选择题
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是
A.AlCl3 B.FeCl3 C.FeCl2 D.CuCl2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市普高高二上学期期中理科化学试卷(解析版) 题型:选择题
下列物质的体积一定是22.4 L的是
A.标准状况下18 g水
B.17 g氨气
C.标准状况下44 g二氧化碳
D.常温常压下2 g氢气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市普高高二上学期期中理科化学试卷(解析版) 题型:选择题
关于钠的叙述中,正确的是
A.钠是银白色金属,硬度很大
B.将金属钠放在石棉网上用酒精灯加热,熔化后剧烈燃烧,产生黄色火焰,生成淡黄色固体
C.金属钠在空气中燃烧,生成氧化钠
D.金属钠的熔点很高
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省乐陵市高二上学期期中考试化学试卷(解析版) 题型:选择题
已知 pOH=-lg[OH-],下列溶液一定呈中性的是
A.由等体积、等物质的量浓度的一元酸跟NaOH溶液混合后所形成的溶液
B.[H+]=1.0×10-7mol·L-1的溶液
C.pH=14-pOH的溶液
D.pH=pOH的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省乐陵市高二上学期期中考试化学试卷(解析版) 题型:选择题
下列金属防腐的措施中,使用外加电流的阴极保护法的是
A.地下钢管连接镁块
B.金属护拦表面涂漆
C.枪炮表面涂上一层油
D.水中的钢闸门连接电源的负极
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东桓台第二中学高二上学期(10月)检测化学试卷(解析版) 题型:选择题
下列物质能通过化合反应直接制得的是( )
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl
A.①②③ B.只有②③ C.只有①③④ D.全部
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东安丘市期中考试高二化学模拟(B)卷(解析版) 题型:填空题
(9分)现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________热反应,且m+n________p(填“>”“=”或“<”)。
(2)减压时,A的质量分数__________。(填“增大”“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________,B的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将__________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_____________________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________;而维持容器内压强不变,充入氖气时,混合物颜色__________(填“变深”“变浅”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com