
【题目】按要求写出对应的式子:
(1)写出电子式:①N2____________②HCN____________③KF____________④Na2O2 ____________⑤Na2S____________ ⑥NH4Cl ________________ 。
(2)写出结构式:①Br2 ____________ ②CO2____________ ③H2O2 ____________ ④CCl4 ____________
(3)用电子式表示形成过程:
①MgCl2_____________________________________________________,②H2O_____________________________。
【答案】![]()
![]()
![]()
![]()
![]()
 Br-Br O=C=O H-O-O-H
Br-Br O=C=O H-O-O-H 

![]()
【解析】
(1)①氮气是共价单质,N原子最外层电子为5个,因而氮原子和氮原子需要形成3对共用电子对,氮气的电子式为![]() 。
。
②HCN是共价化合物,C原子最外层为4个电子,碳原子与氢原子形成1对共用电子对,碳原子与氮原子形成3对共用电子对,因而HCN的电子式为![]() 。
。
③KF是离子化合物,钾离子的电子式为K+,氟离子的电子式为![]() ,因而氟化钾的电子式为
,因而氟化钾的电子式为![]() 。
。
④过氧化钠是离子化合物,由钠离子与过氧根离子构成,钠离子电子式为Na+,过氧根离子电子式为![]() ,因而过氧化钠的电子式为
,因而过氧化钠的电子式为![]() 。
。
⑤硫化钠是离子化合物,由2个钠离子和1个硫离子构成,钠离子电子式为Na+,硫离子电子式为![]() ,因而硫化钠的电子式为
,因而硫化钠的电子式为![]() 。
。
⑥氯化铵是离子化合物,由铵根离子和氯离子构成,铵根离子的电子式为 ,氯离子电子式为
,氯离子电子式为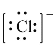 ,因而氯化铵的电子式为
,因而氯化铵的电子式为 。
。
(2)①Br原子最外层7个电子,溴原子与溴原子形成一对共用电子对,因而结构式为Br-Br。
②碳原子最外层为4个电子,氧原子最外层为6个电子,因而碳原子与每个氧原子形成2对共用电子对,即形成碳氧双键,因而二氧化碳的结构式为O=C=O。
③过氧化氢中存在过氧键,氧原子和氧原子之间形成1对共用电子对,氧原子与氢原子也形成1对共用电子对,因而过氧化氢的结构式为H-O-O-H。
④碳原子最外层为4个电子,与4个氯原子各形成1对共用电子对,即形成4个碳氯单键,因而其结构式为 。
。
(3)①氯化镁是离子化合物,其电子式为![]() ,其形成过程可描述为两个氯原子各得到一个来自于镁原子的最外层电子,因而电子式表示形成过程为
,其形成过程可描述为两个氯原子各得到一个来自于镁原子的最外层电子,因而电子式表示形成过程为![]() 。
。
②H2O是共价化合物,其电子式为![]() ,氧原子和两个氢原子各形成1对共用电子对,用电子式表示的形成过程为
,氧原子和两个氢原子各形成1对共用电子对,用电子式表示的形成过程为![]() 。
。


科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
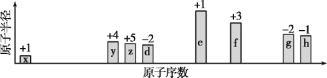
根据判断出的元素回答问题:
(1)h在周期表中的位置是________。
(2)比较d、f离子半径大小(用化学式表示,下同):____>____。比较g、h的最高价氧化物对应水化物的酸性强弱:____>____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 甲基橙显黄色的溶液: Na+、CO32-、NO3-、SO32-
B. 在由水电离出的c(H+)=1×10-12mol/L的溶液:Fe3+、ClO-、Na+、SO42-
C. PH=7的溶液中:K+、Al3+、NO3-、SO![]()
D. 使酚酞变红的溶液中:K+、Na+、I-、AlO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑾ | ⑿ |
(1)写出下列元素的元素符号:①_____②____⑾____
(2)在这些元素中,最活泼的金属元素是____,最活泼的非金属元素是____,最不活泼的元素是____。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是__________,碱性最强的是___________,呈两性的氢氧化物是____________。
(4)在③与④的单质中,化学性质较活泼的是______,判断依据是_______________;在⑧与⑿ 的单质中,化学性质较为活泼的是______,判断依据是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )

A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 共价化合物中不可能含有离子键,一定含有共价键
B. 阴阳离子之间通过静电引力形成的化学键叫离子键
C. 含有共价键的化合物不一定是共价化合物
D. 含有离子键的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是( )

A. 铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生
B. 电路中的电流方向由锌片流向铜片
C. 其能量转化的形式主要是“化学能→电能→光能”
D. 如果将稀硫酸换成柠檬汁,LED灯将不会发光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表一部分,列出了十种元素在周期表中的位置:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
3 | ① | ③ | ④ | ⑨ | ||||
4 | ② | ⑩ |
请回答下列问题:
(1)在上述元素中,非金属性最强的是________(填元素名称),原子半径最大的是_____(填元素符号),⑧与⑩两者核电荷数之差是_____________。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_______________(填物质化学式)。
<>(3)⑤和⑦可以形成一种温室气体,用电子式表示其形成过程____________________________。(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:___________,该物质所含化学键类型为__________________,写出X与水反应的离子方程式_____________________ 0.1mol X与水反应转移电子数为 _______________。
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com