
【题目】下列化学方程式书写不正确的是
A.苯与浓硝酸反应:![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
B.苯酚钠溶液与二氧化碳反应:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +Na2CO3
+Na2CO3
C.溴乙烷消去反应:CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr +H2O
CH2=CH2↑+NaBr +H2O
D.乙醛与银氨溶液反应:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+ 2Ag↓+ 3NH3 +H2O
CH3COONH4+ 2Ag↓+ 3NH3 +H2O
【答案】B
【解析】
A. 苯与浓硝酸反应生成硝基苯和水,反应的化学方程式为:![]() +HNO3
+HNO3![]()
![]() +H2O,选项A正确;
+H2O,选项A正确;
B. 苯酚钠溶液与二氧化碳反应生成苯酚和碳酸氢钠,反应的化学方程式为:![]() +CO2+H2O→
+CO2+H2O→![]() +NaHCO3,选项B不正确;
+NaHCO3,选项B不正确;
C. 溴乙烷在氢氧化钠的乙醇溶液中加热发生消去反应生成乙烯、溴化钠和水,反应的化学方程式为:CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr +H2O,选项C正确;
CH2=CH2↑+NaBr +H2O,选项C正确;
D. 乙醛与银氨溶液反应生成乙酸铵、银、氨气和水,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+ 2Ag↓+ 3NH3 +H2O,选项D正确;
CH3COONH4+ 2Ag↓+ 3NH3 +H2O,选项D正确;
答案选B。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
(1)铷位于元素周期表的第________周期________族。
(2)关于铷的下列说法中不正确的是________(填数字序号)。
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳
③Rb2O2与水能剧烈反应并释放出O2
④它是极强的还原剂 ⑤RbOH的碱性比同浓度的NaOH弱
(3)现有铷和另一种碱金属形成的合金5 g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱金属可能是_______________(填元素符号)。
(4)铷久置于空气中,最终变成产物是_____________。
A、Rb2O B、Rb2O2 C、Rb2CO3 D、RbHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构简式为![]() ,关于该有机物下列叙述正确的是
,关于该有机物下列叙述正确的是
A. 不能使酸性KMnO4溶液褪色
B. 不能使溴水褪色
C. 在加热和催化剂作用下,最多能和4 mol H2反应
D. 易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20mL0.1mol·L-1H2C2O4溶液 | 30mL0.1 mol·L-1KMnO4溶液 |
② | 20mL0.2mol·L-1H2C2O4溶液 | 30mL0.1mol·L-1KMnO4溶液 |
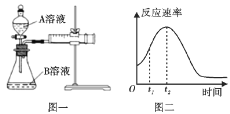
(1)该实验探究的是___因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是___(填实验序号)。
(2)若实验①在2min末收集了2.24mLCO2(标准状况下),则在2min末,c(MnO4-)__mol·L-1(假设混合液体积为50mL)。
Ⅱ.一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
下列描述能说明该可逆反应达到化学平衡状态的有___。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3mol H-H键断裂,有6mol N-H键形成
D.c(N2):c(H2):c(NH3)=1:3:2
E.NH3的质量分数不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:6H2(g)+2CO2(g) ![]() CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是 ( )
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是 ( )
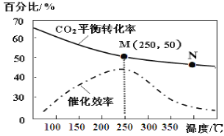
A.M点的正反应速率V正大于N点的逆反应速率V逆
B.若投料比n(H2):n(CO2)=4:1,则图中M点乙烯的体积分数约为5.88%
C.250℃,催化剂对CO2转化率影响最大
D.当温度高于250℃,升高温度,平衡逆向移动导致催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,AgCl(s)Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是
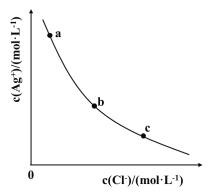
A.a、b、c三点对应的Ksp 不相等
B.AgCl在c点的溶解度比b点的大
C.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D.b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定的误差要求小于0.1%,若用20.00 mL0.2000mol·L-1盐酸滴定20mL0.2000mol·L-1NaOH溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)( )
A. 4.3~9.7B. 3.7~10.3C. 4.0~10.0D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com