
【题目】一定温度下,AgCl(s)Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是
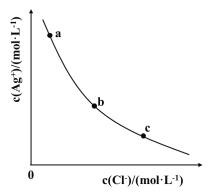
A.a、b、c三点对应的Ksp 不相等
B.AgCl在c点的溶解度比b点的大
C.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D.b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化
科目:高中化学 来源: 题型:
【题目】X溶液中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种成几种,取该溶液进行实验,实验内容和相关数据
中的一种成几种,取该溶液进行实验,实验内容和相关数据![]() 气体体积在标准状况下测定
气体体积在标准状况下测定![]() 如下:
如下:

![]() 溶液中一定不存在的离子是______。
溶液中一定不存在的离子是______。
![]() 已知气体D为NO,加入过量
已知气体D为NO,加入过量![]() 和
和![]() 溶液时,发生反应的离子方程式为______。
溶液时,发生反应的离子方程式为______。
![]() 溶液中
溶液中![]() ______
______![]() ,
,![]() ______
______![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究Al与CuCl2溶液反应,实验如下:下列说法不正确的是( )
实验 | 现象 |
| a.Al片表面附着蓬松的红色固体 b.产生无色气体,起始速率较慢,之后加快 c.反应放热 d.烧杯底部产生少量不溶于稀盐酸的白色沉淀 e.溶液pH降低 |
A.无色气体是H2
B.实验中影响化学反应速率的因素只有两个,分别是浓度和温度
C.白色沉淀的出现与氧化还原反应有关
D.将铝片改为铝粉会加快化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式书写不正确的是
A.苯与浓硝酸反应:![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
B.苯酚钠溶液与二氧化碳反应:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +Na2CO3
+Na2CO3
C.溴乙烷消去反应:CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr +H2O
CH2=CH2↑+NaBr +H2O
D.乙醛与银氨溶液反应:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+ 2Ag↓+ 3NH3 +H2O
CH3COONH4+ 2Ag↓+ 3NH3 +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出142.9kJ热量。则H2燃烧的热化学方程式为_____
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g)![]() 2NH3(g);ΔH=-92.4kJ/mol
2NH3(g);ΔH=-92.4kJ/mol
①一定条件下,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中加入催化剂引起反应速率变化的时间段是____(填,如0~t1等)。
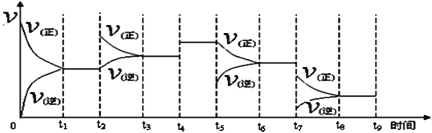
②生产中为提高反应速率和H2的转化率,下列措施可行的是___(填字母)。
A.向装置中充入过量N2 B.及时将合成的氨气从装置中分离出来
C.使用更高效的催化剂 D.升高温度
③温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物丙可由有机物甲和乙在一定条件下反应制得:
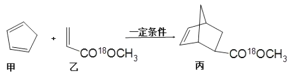
下列说法正确的是
A.丙在碱性条件下水解生成 和CH318OH
和CH318OH
B.甲分子中所有原子共平面
C.乙的化学式是C4H518OO
D.甲与乙生成丙的反应属于加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数![]() (X)=
(X)=![]() 与pH的关系如图所示:
与pH的关系如图所示:

下列说法正确的是
A. 反应HCO3-![]() H++CO32-的lgK=-6.4
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某![]() 样品中含有
样品中含有![]() 、
、![]() 和
和![]() 三种杂质的一种或两种,现将
三种杂质的一种或两种,现将![]() 样品加入足量水,样品全部溶解,再加入过量的
样品加入足量水,样品全部溶解,再加入过量的![]() 溶液得到9克沉淀,对样品所含杂质的正确判断是
溶液得到9克沉淀,对样品所含杂质的正确判断是![]()
A.肯定没有![]()
B.肯定没有![]() 和
和![]()
C.肯定没有![]() ,可能有
,可能有![]()
D.肯定没有![]() ,可能有
,可能有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气和氨水在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH)2]和氯化铵混合固体制取氨气,写出反应的化学方程式___________。
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。
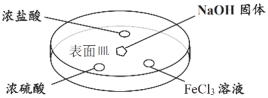
①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl3溶液
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl3液滴中出现的现象是___________,发生反应的离子方程式是_________。
(4)利用氨水可以将大气污染物SO2吸收并生产氮肥,原理如图所示:
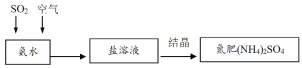
分析上述生产原理,在下列表格中填写该生产过程中利用的SO2的化学性质并进行理论论证
SO2的化学性质 | 理论论证 |
______ | ______ |
______ | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com