
����Ŀ������ʱ����H2CO3��Һ����μ���NaOH��Һ����Һ��H2CO3��HCO3-��CO32-�����ֲַ�����![]() (X)=
(X)=![]() ��pH�Ĺ�ϵ��ͼ��ʾ��
��pH�Ĺ�ϵ��ͼ��ʾ��

����˵����ȷ����
A. ��ӦHCO3-![]() H����CO32-��lgK=-6.4
H����CO32-��lgK=-6.4
B. pH�T8����Һ�У�c��Na����>c��HCO3-��
C. NaHCO3��Һ�е���������������Һ�����ԣ�c��Na�����Tc��Cl-��
D. ��pH=6.4����Һ�еμ�NaOH��Һ��pH=8����Ҫ���������ӷ�Ӧ��HCO3-��OH-�TCO32-��H2O
���𰸡�B
��������
A��pH�T6.4ʱ��c��HCO3-���Tc��H2CO3�����������ӦH2CO3![]() H++HCO3-��lgK��
H++HCO3-��lgK��
B�����ݵ���غ������
C�����ݵ���غ������
D��pH=8ʱ��̼��ת��Ϊ̼���������Ҫ���������ӷ�ӦΪH2CO3��OH-=HCO3-��H2O��
A��pH�T6.4ʱ��c��HCO3-���Tc��H2CO3������ӦH2CO3![]() H++HCO3-��lgK�Tlgc(H+)=lg10-6.4=һ6.4����A�����
H++HCO3-��lgK�Tlgc(H+)=lg10-6.4=һ6.4����A�����
B��pH�T8����Һ�У�c��H����<c��OH-�������ݵ���غ���c��Na+����c��H�����Tc��C1-��ʮc��HCO3-����2c��CO32-����c��OH-��������c��Na+��>c��C1-��ʮc��HCO3-����2c��CO32-������c��Na����>c��HCO3-��,��B��ȷ��
C����NaHCO3��Һ�е���������������Һ������ʱ��c��H�����Tc��OH-�������ݵ���غ���c��Na+����c��H�����Tc��C1-��ʮc��HCO3-����2c��CO32-����c��OH-������c��Na+���Tc��C1-��ʮc��HCO3-����2c��CO32-������C�����
D��pH�T6.4����Һ�к��е����ʵ�����NaHCO3��H2CO3����ͼ���֪��pH=8ʱ��Һ��HCO3-��������������H2CO3������Ҫ���������ӷ�ӦΪH2CO3��OH-=HCO3-��H2O����D�����
��ѡB��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ���Na2O2��H2O��Ӧ������ȡ����O2��������װ����ȡO2����ʾNa��O2�е�ȼ��ʵ�飮
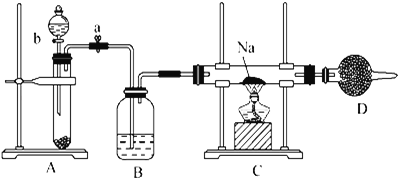
��ش��������⣺
(1)д��Aװ���з�Ӧ�Ļ�ѧ����ʽ_____��
(2)Bװ����ʢ�ŵ��Լ���_____��
(3)Dװ����ʢ�ŵ��Լ���_____����������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ����ˮ������������������ˮ��pH��5.0��6.0֮�䣬ͨ���������Fe(OH)3���壬Fe(OH)3��������������ã�������ˮ�е������ʹ�������������ˮ�����ã���ԭ����ͼ��ʾ������˵����ȷ����

A. ʯī�缫�Ϸ���������Ӧ
B. ����ͼʾ������AΪCO2
C. Ϊ��ǿ��ˮ�ĵ���������������ˮ�м��������Ҵ�
D. ����ȼ�ϵ����CO32�������һ���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ײʱ����ȫ�����з�����Ӧ��10NaN3��2KNO3=K2O��5Na2O��16N2��������˵������ȷ����( )
A.��ԭ�ԣ�NaN3 > N2
B.����65 g NaN3�μӷ�Ӧ�������ɵ�N2�����ʵ���Ϊ1.6 mol
C.ÿת��1 mol���ӣ������ɱ�״����N2�����Ϊ35.84 L
D.����ԭ��N�뱻������NΪ15 ��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����ֵ������˵����ȷ����
A. �ڱ�״���£�4.48Lˮ�к��еķ�����ĿΪ0.2NA
B. 0.1mol![]() ���Ӻ��еĵ��ӡ���������Ϊ1.0NA
���Ӻ��еĵ��ӡ���������Ϊ1.0NA
C. һ�������£�0.1mol![]() ��0.3mol
��0.3mol![]() ��ַ�Ӧ���0.1NA������
��ַ�Ӧ���0.1NA������
D. �����ʵ���Ϊ0.1mol��CaO��![]() ������У�������������Ϊ0.2NA
������У�������������Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����500mL����BaCl2��KCl�Ļ����Һ�ֳ�2�ȷݣ�ȡһ�ݼ��뺬a mol �����Ƶ���Һ��ǡ��ʹ��������ȫ��������ȡһ�ݼ��뺬b mol ����������Һ��ǡ��ʹ��������ȫ�����������Һ�м�����Ũ��Ϊ:
A.0.1(b-2a)mol/LB.10(b-2a)mol/L
C.10(2a-b)mol/LD.4(b-2a)mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ę́���д����������з�����ζ������X����ṹ����ͼ��ʾ������˵����ȷ����
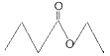
A. X�������Ҵ�
B. ���������Ķ���������X��ˮ��
C. X��ȫȼ�պ�����CO2��H2O�����ʵ�����Ϊ1��2
D. ����ʽΪ![]() �ҹ�������X��ͬ�����ʹ���5��
�ҹ�������X��ͬ�����ʹ���5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ʵ��������ȷ����
A. ��Ũ��ˮ�еμӱ���![]() ��Һ�������Ƶ�
��Һ�������Ƶ�![]() ����
����
B. Ϊ��ȥMg(OH)2 ����������Ca(OH)2�����ñ���MgCl2��Һ���ϴ�ӣ���ˮϴ������
C. ����Һ X �м����������ᣬ������ɫ��ζ���壬������ͨ�����ʯ��ˮ��������ɫ������˵����Һ X �к���CO32��
D. ±����Y��NaOH����Һ���Ⱥָ������£��ٵμ�AgNO3 ��Һ��������ɫ������˵��±����Y�к�����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��ݸ�����ͼ�������жϣ���ȷ����
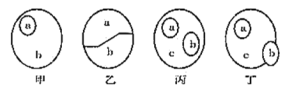
A. ��ֲ��ϸ���ڣ���ͼ��a��b���Ա�ʾ���ۺ������ǵĹ�ϵ
B. ������a��b�ֱ����DNA��RNA������ͼ���Դ��������ڵĺ���
C. ��ͼ��a��b��c�ɷֱ��ʾ��֬���̴���֬��֮��Ĺ�ϵ
D. ��ͼa��b��c�ɷֱ��ʾ�����ʡ����غ�ø֮��Ĺ�ϵ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com