
����Ŀ�������Ƿdz���Ҫ����Դ�ͻ���ԭ�ϣ���ش���������.
(1)����ͼ��ʾ��װ�â�Ϊ����ȼ�ϵ��(�������ҺΪH2SO4��Һ)��ͨ��װ�â�ʵ��������ͭ��

��a��Ӧͨ��______(�CH4����O2��)��b���缫�Ϸ����ĵ缫��Ӧʽ��___________��
�ڵ�ƽ�����װ�â�����Һ��pH______(��д�������С�����䡱����ͬ)��װ�â���Cu2�������ʵ���Ũ��_______��
����ʵ������Т��е�ͭƬ����������2.56g�����������������CH4�����(��״��)______L��
��2������װ�â��е����缫����Ϊʯī���Ե缫��
��д��װ�â��з������ܻ�ѧ��Ӧ��ʽ________________________________��
�����â���200 mL 0.05 mol��L��1��CuSO4��Һ��һ��ʱ�����Һ�е�Cu2+ǡ����ȫ�������ָ������£���ҺpH=__________(���Ե���������Һ����仯)�����뽫�����������Һ�ָ�Ϊ����ǰ����Һ��ͬ�����Լ���һ��������__________(�����)��
a��Cu b��CuO c��Cu(OH)2 d��CuSO4
���𰸡�CH4 O2+4H++4e-=2H2O ��� ���� 0.224 2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4 1 b
2Cu+O2��+2H2SO4 1 b
��������
(1)����Fe���϶�Cu����Cu������������Ӧ����������b�缫��������a�缫��������CH4��a��ͨ�룬O2��b��ͨ�룬�����������������Һ����b����ӦʽΪO2+4H��+4e��=2H2O��
����𰸣�CH4��O2+4H��+4e��=2H2O��
��װ�â����ܷ�ӦΪ��CH4��2O2=CO2��2H2O��ˮ������Һ���������Һ��pH���ƹ����������缫���ɵ�ͭ���Ӻ����ĵ�ͭ������ȣ�ͭ����Ũ�Ȳ��䣻
����𰸣������
��CH4ȼ�ϵ���еĻ�ѧ����ʽΪCH4+2O2=CO2+2H2O���ɵ����غ��CH4~4Cu��2.56 g Cu�����ʵ���Ϊ0��04 mol��������CH40��01 mol���ڱ�״���µ����Ϊ0��01mol��22��4 L��mol-1=0.224L��
����𰸣�0.224L
��2��������װ�â��е����缫����Ϊʯī���Ե缫������������Cu 2+ +2e - �TCu���������������ӷŵ磬4OH - -4e - �T2H2O+O 2 �����ܻ�ѧ��Ӧ��ʽ2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4
2Cu+O2��+2H2SO4
����𰸣�2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4
2Cu+O2��+2H2SO4
����Һ��Cu2+ǡ����ȫ��Ӧ��������������n��Cu��=0.2L��0.05 mol/ L=0.01 mol�����ɵ�����Ϊ0.01 mol��������Ϊ0.02 mol��c��H+��=0.02 mol/0.2L=0.1 mol/ L��pH=1���������ͭ��Һ����Һ�е�Cu2+ǡ����ȫ��Ӧ��������ʽΪ2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4��Ҫ��ָ�������ǰ����Һ��ͬ��Ӧ����CuO��
2Cu+O2��+2H2SO4��Ҫ��ָ�������ǰ����Һ��ͬ��Ӧ����CuO��
����𰸣�1��b


 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾװ�ý���ʵ�飬��Ӧ�����㹻��ʱ���װ��II��ʵ��������ȷ����
�� | �� | �� | II��ʵ������ |
| |
A | Ũ���� | ̼��� | ���з�̪��ϡ̼������Һ | ��Һ�ɺ�ɫ��Ϊdz��ɫ | |
B | Ũ��ˮ | ������ | ����������Һ | ����������ɫ���� | |
C | ������ | �Ҵ���Ũ���� | ����̼������Һ | ��Һ�ֲ㣬�ϲ�Ϊ��״Һ�� | |
D | NH4Cl��Һ | NaAlO2��Һ | ��ɫʯ����Һ | ��Һ����ɫ��Ϊ��ɫ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͨ�����������Լ������м�ȩ�ĺ������ô�������ԭ��
��ͼ��ʾ��

��1����װ�õ���Ҫ����ת����ʽ��_______________��bΪ______���������ĵ缫��ӦʽΪ_________________��
��2���ڴ��������������У��������Һ�����Ũ��___________���������С�������䡱��������·��ת��0.2 mol����ʱ���������ڲμӷ�Ӧ��HCHOΪ_______g��
������ͼװ�õ���������Һ����ȡ������������������������أ������ڵ������ӽ���Ĥֻ����������ͨ���������ӽ���Ĥֻ����������ͨ������

��1���õ��۵���������_____��Ӧ�������������ԭ������
��2���Ƶõ�������Һ�ӳ���_______���A������D����������������ԭ��________________________________________________�����û�ѧ��������ֽ��ͣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���õ����ز�����ͭ��װ��ͼ��ʾ�˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4������˵������ȷ����

A. �ù����ǽ�̫����ת��Ϊ��ѧ�ܵĹ���
B. GaN���淢��������Ӧ��2H2O��4 e��=== O2����4H��
C. Cu����ķ�Ӧ�ǣ�CO2��8e����6H2O === CH4��8OH
D. H+�����ӽ���Ĥ��������Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ͼ��ʾʵ�飬��ȷ��ij��������к��� CH2=CH2 ��SO2��
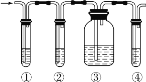
ʵ�����ṩ���Լ��У�A.Ʒ����ҺB.NaOH ��ҺC.Ũ����D.���� KMnO4 ��Һ�Իش��������⣺
(1)д��ͼ�Т٢ڢۢ� װ��ʢ���Լ���˳��Ϊ( �������й��Լ����������ո���) ___________��___________��___________��___________��
(2)��˵����������д���SO2 ��������___________��
(3)��ȷ����������д�����ϩ��������___________��
(4)��ϩ����ˮ��Ӧ�Ļ�ѧ����ʽΪ_______���÷�Ӧ�ķ�Ӧ����Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Cr2O3����Ҫ����ұ�����������л���ѧ�ϳɵĴ�����.��ҵ�����Ը�����[��Ҫ�ɷ�ΪFe(CrO2)2��������Al2O3��SiO2������]Ϊ��Ҫԭ�Ͻ�������������Ҫ�����������£�

��1���Ǹ�������[Fe(CrO2)2]��Cr�Ļ��ϼ���___________��
��2������ʱ����Ҫ��ӦΪ��4FeO��Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2�����б�������Ԫ��Ϊ___��ÿ����32g Fe2O3��ת�Ƶ��ӵ����ʵ���Ϊ_______���ò��費��ʹ���մ�������ԭ����_______��
8Na2CrO4+2Fe2O3+8CO2�����б�������Ԫ��Ϊ___��ÿ����32g Fe2O3��ת�Ƶ��ӵ����ʵ���Ϊ_______���ò��費��ʹ���մ�������ԭ����_______��
��3������I����������ϴ�ӣ�����ʵ������ϴ�ӳ����IJ�����__________��
��4�������������Ƶķ�Ӧ��ת��Ϊ��������ƣ���Ӧ�����ӷ���ʽΪ___________�������г�Al(OH)3���_______���ѧʽ����
��5��ij������448 kg�������[��Fe(CrO2)280%]�Ʊ�Cr2O3�����յõ���Ʒ182.4 kg������Ϊ______��
��6��Cr3+Ҳ��һ�����ԣ�����Ⱦˮ�壬������Ҫ��ȥ��Һ�ж����Cr3+������pH����Ϊ_______������ʹ�����ӳ�����ȫ (��֪������Ũ��С��1��10��5mol/Lʱ�����ʹ���ȫ�� Cr(OH)3��Ksp=1.0��10��32)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.2mol/LһԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ������˵����ȷ����

A. HA��ǿ��
B. �û��ҺpH=7
C. ͼ��x��ʾHA��Y��ʾOH-��Z��ʾH+
D. �û����Һ�У�c(A-)+c(Y)=c��Na+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��0.4 molij��������Ϊ9.8 L����������Ħ�����Ϊ____________��
��2���б�״���µ���������:��6.72 L CH4����3.01��1023��H2���ӣ���3.4 g H2S����0.2 mol NH3������������Ӵ�С��˳��Ϊ:_________________������ţ���
��3����״���£����1.92��ij��������Ϊ672 mL������������Է�������Ϊ__________
��4��ʵ������Na2CO3��10H2O��������0.5mol/L��Na2CO3��Һ970mL��Ӧ��ȡNa2CO3��10H2O��������___________��
��5��ijѧ������12mol��L��1Ũ���������ˮ����500 mL 0.3 mol��L��1��ϡ���ᡣ
����ѧ����Ҫ��ȡ________mL����Ũ����������ơ�
������ʵ������ᵼ�������Ƶ�ϡ��������ʵ���Ũ��ƫС����__________������ţ���
a.����Ͳ��ȡŨ����ʱ���ӹ۲찼Һ��
b.����ȡŨ�������Ͳ����ϴ�ӣ�����ϴ��Һת�Ƶ�����ƿ��
c.ϡ��Ũ����ʱ��δ��ȴ�����¼�ת�Ƶ�����ƿ��
d. ���ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ
e.����ƿϴ�Ӹɾ���δ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ʽ��ͼ��ʾ��Na��NaOH��NaHCO3�ֱ�������ʵ����ĸ�����ǡ�÷�Ӧʱ��Na��NaOH��NaHCO3�����ʵ���֮��Ϊ(����)
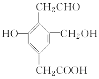
A. 3��3��2B. 3��2��1
C. 1��1��1D. 3��2��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com