
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位。请回答下列问题:

(1)A、B分别是________、________。
(2)如果Ⅰ是人和动物细胞的主要能源物质,则X的名称是________。
(3)P经________方式形成Ⅳ,连接两个P的化学键的结构简式是________。Ⅳ多种多样,从P分析原因是____________________。
(4)大分子物质Ⅰ~Ⅴ中,具有物种特异性的是________。
(5)由小分子物质X、Y、Z、P生成大分子物质Ⅰ、Ⅱ、Ⅲ、Ⅳ的过程中,有一共同的生成物是________。
(6)相同质量的Ⅴ氧化分解时释放的能量远远多于Ⅰ,原因是Ⅴ中________含量高。
【答案】N、P N 葡萄糖 脱水缩合 —NH—CO— 构成Ⅳ的氨基酸的种类不同,数目不同,排列顺序不同 Ⅱ、Ⅲ、Ⅳ 水 C、H
【解析】
本题以“细胞内某些有机物的元素组成和功能关系图”为载体,考查学生对细胞内的有机大分子的化学组成及功能等相关知识的识记和理解能力,以及获取信息、分析问题的能力。
(1) 依题意并结合图示分析可知:携带遗传信息的是核酸,其中主要分布于细胞核中的Ⅱ是DNA,Y是组成DNA的基本单位脱氧核苷酸,主要分布于细胞质中的Ⅲ是RNA,Z是组成RNA的基本单位核糖核苷酸。核糖核苷酸与脱氧核苷酸都是由C、H、O、N、P组成,因此A表示N、P。承担生命活动的Ⅳ是蛋白质,P是组成蛋白质的基本单位氨基酸,氨基酸的基本组成元素是C、H、O、N,所以B表示N。
(2) 如果Ⅰ是人和动物细胞的主要能源物质,则Ⅰ是糖原,X是组成糖原的基本单位葡萄糖。
(3) P是氨基酸,Ⅳ是蛋白质。P经脱水缩合方式形成Ⅳ,连接两个P的化学键为肽键,其结构简式是-NH-CO-。Ⅳ多种多样,从P分析,其原因是构成Ⅳ的氨基酸的种类、数目、排列顺序不同。
(4) 大分子物质Ⅰ~Ⅴ依次表示淀粉或糖原、DNA、RNA、蛋白质、脂肪,其中具有物种特异性的是Ⅱ、Ⅲ、Ⅳ。
(5)综上分析,小分子物质X、Y、Z、P都是通过脱水缩合反应生成相应的大分子物质Ⅰ、Ⅱ、Ⅲ、Ⅳ,此过程都有水生成。
(6) Ⅰ为糖类中的淀粉或糖原,Ⅴ为脂肪。由于脂肪中C、H的含量远远高于糖类,而氧的含量远远低于糖类,所以相同质量的脂肪氧化分解时释放的能量远远多于糖类。


科目:高中化学 来源: 题型:
【题目】某温度下Kw=10-13,在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,下列说法正确的是( )
A. 若所得混合液为中性,且a=12,b=2,则Va∶Vb=1∶1
B. 若所得混合液为中性,且a+b=12,则Va∶Vb=100∶1
C. 若所得混合液pH=10,且a=12,b=2,则Va∶Vb=1∶9
D. 若所得混合液pH=10,且a=12,b=2,则Va∶Vb=101∶99
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,可逆反应mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,一定达到平衡的标志是( )
pC(g)+qD(g),当m、n、p、q为任意整数时,一定达到平衡的标志是( )
①体系的温度不再改变 ②体系的压强不再改变
③各组分的浓度不再改变 ④各组分的质量分数不再改变
⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
⑥单位时间内m mol A发生断键反应,同时p mol C也发生断键反应
A. ③④⑤⑥B. ①③④⑥C. ②③④⑥D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中说明乙醇作为燃料的优点的是( )
①燃烧时发生氧化还原反应
②充分燃烧的产物不污染环境
③乙醇是一种可再生能源
④燃烧时放出大量热量
A.①②③B.①②④C.①③④D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镧系为元素周期表中第ⅢB族、原子序数为57至71的元素。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:_____。
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为_______________。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是_______(填元素名称)。
几种镧系元素的电离能(单位:kJ·mol-1)
元素 | I1 | I2 | I3 | I4 |
Yb(镱) | 604 | 1217 | 4494 | 5014 |
Lu(镥) | 532 | 1390 | 4111 | 4987 |
La(镧) | 538 | 1067 | 1850 | 5419 |
Ce(铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为_______________(用元素符号表示)。
②元素Al也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为________,分子中所含化学键类型有______________(填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有______个氧原子;已知晶胞参数为a pm,密度为ρg·cm-3,NA=________ (用含a、ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g)![]() 2C(g)+zD(g)。若2s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g)。若2s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A. v(C)=v(A)=0.2 mol·L-1·s-1
B. z=3
C. B的转化率为75%
D. 反应前与2 s后容器的压强比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1 mol DAx与足量的A2C反应生成44.8 L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T→W(未配平),测得各物质的浓度如表所示。
物质 | T | G | W |
10 min时,c/(mol/L) | 0.5 | 0.8 | 0.2 |
20 min时,c/(mol/L) | 0.3 | 0.2 | 0.6 |
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,该化合物的化学式为_________。
(2)B、C、D、E的简单离子中,离子半径由大到小排序为__________(用离子符号表示)。
(3)J、L是由A、B、C、E四种元素组成的两种常见酸式盐,J、L混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式__________;J、L中能使酸性高锰酸钾溶液褪色的是_______(填化学式)。
(4)B2A4C2碱性燃料电池放电效率高。该电池放电时生成B2和A2C,正极反应式为________;电池工作一段时间后,电解质溶液的pH_____(填“增大”“减小”或“不变”)。
(5)由A、B、C、D四种元素组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示,已知M耐高温。
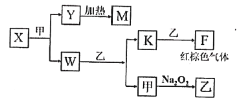
①X的电子式为______。
②已知W与乙反应生成K和甲是某重要化工生产步骤之一,提高其反应速率的方法除增大反应物浓度、增大压强外,还有______、______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com