
| A. | C3N4 晶体是分子晶体 | |
| B. | C3N4 晶体中微粒间通过离子键结合 | |
| C. | C3N4 晶体中C-N键的键长比金刚石中C-C键的键长要长 | |
| D. | C3N4 晶体中每个C原子连接4个N 原子,而每个N原子连接3个C原子 |
分析 C3N4晶体具有比金刚石还大的硬度,且原子间均以单键结合,可知为原子晶体,只存在C-N共价键,空间为网状结构,结合原子半径可比较共价键的键长,以此来解答.
解答 解:A.因硬度比金刚石大,则C3N4 晶体是原子晶体,故A错误;
B.C3N4 晶体中原子间均以单键结合,不存在离子键,故B错误;
C.C的原子半径大于N的原子半径,则C3N4 晶体中C-N键的键长比金刚石中C-C键的键长要短,故C错误;
D.C原子周围有4个单电子,N原子周围有3个单电子,则C3N4 晶体中每个C原子连接4个N 原子,而每个N原子连接3个C原子,且原子间均以单键结合,形成空间网状结构,故D正确;
故选D.
点评 本题考查晶体及化学键,为高频考点,把握习题中的信息、晶体类型、晶体中作用力为解答的关键,侧重分析与应用能力的考查,注意化学键的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.400mol•L-1 | B. | 0.300mol•L-1 | C. | 0.200mol•L-1 | D. | 0.100mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
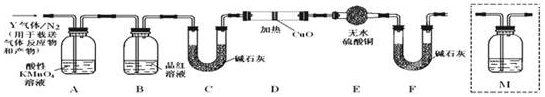
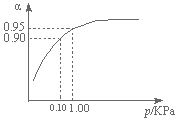
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成1 mol NaNO3需消耗0.4 mol KMnO4 | |
| B. | 反应过程中溶液的pH减小 | |
| C. | 该反应中NO${\;}_{2}^{-}$被还原 | |
| D. | X可以是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 熔点℃ | 沸点℃ | 密度(g/cm3) | |
| Na | 97.8 | 882.9 | 0.97 |
| K | 63.7 | 774 | 0.86 |
| NaCl | 801 | 1413 | 2.165 |
| KCl | 770 | 1500(升华) | 1.984 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
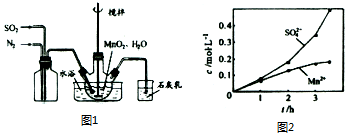
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
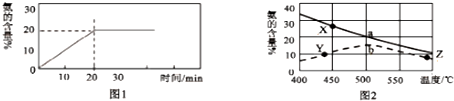
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com