
【题目】化合物G是一种药物合成中间体,其合成路线如图所示![]() 部分反应条件已省略
部分反应条件已省略![]() :
:
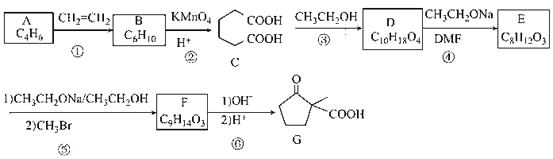
已知:①![]() ;
;
②![]()
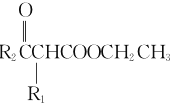
![]() 。
。
回答下列问题:
(1)![]() 中官能团的名称为________。
中官能团的名称为________。
(2)A是一种烯烃,其系统命名为________。
(3)由C生成D的化学方程式为________。
(4)E的结构简式为________。
(5)第⑤步反应的反应类型为________。
(6)同时满足下列条件的C的同分异构体有________种![]() 不含立体异构
不含立体异构![]() ,其中核磁共振氢谱显示有3组峰,且峰面积之比为2:2:1的结构简式为________。
,其中核磁共振氢谱显示有3组峰,且峰面积之比为2:2:1的结构简式为________。
①![]() 该物质能与
该物质能与![]() 反应。
反应。
②![]() 该物质与银氨溶液反应生成
该物质与银氨溶液反应生成![]() 。
。
(7)参考G的合成路线,设计以乙酸乙酯和溴乙烷为原料![]() 其他试剂任选
其他试剂任选![]() ,制备
,制备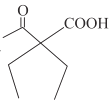 的合成路线:________。
的合成路线:________。
【答案】羰基、羧基 ![]() ,
,![]() 丁二烯
丁二烯 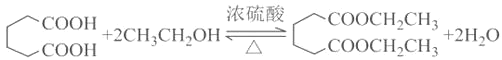
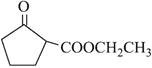 取代反应
取代反应 ![]()
![]()
![]()
![]()
![]()
![]()

【解析】
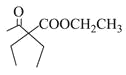
根据C的结构结合信息分析可知B为环己烯,反推A为![]() ,根据转化关系可知D为己二酸二乙酯,由信息
,根据转化关系可知D为己二酸二乙酯,由信息![]() 可知E为
可知E为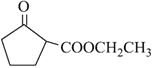 ;由G可知F为:
;由G可知F为: 。
。
(1)G中官能团为羰基、羧基;
(2)A的分子式为![]() ,A为烯烃且A的不饱和度为2,故A为1,
,A为烯烃且A的不饱和度为2,故A为1,![]() 丁二烯;
丁二烯;
(3)![]() 为酯化反应,反应的化学方程式为
为酯化反应,反应的化学方程式为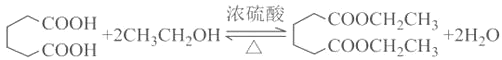 ;
;
(4)由信息②和E的分子式可知,E的结构简式为 ;
;
(5)![]() 是酯基的水解以及酸化,因此
是酯基的水解以及酸化,因此![]() 增加了一个甲基,对比条件可知,甲基来自
增加了一个甲基,对比条件可知,甲基来自![]() ,因此该反应为取代反应;
,因此该反应为取代反应;
(6)①1mol该物质能与
②1mol该物质与银氨溶液反应生成![]() ,可知,同分异构体中含有两个甲酸酯基,因此该问题就是丁烷上的二取代问题,由定一移一得共有9种,其中核磁共振氢谱显示有3组峰,且峰面积之比为
,可知,同分异构体中含有两个甲酸酯基,因此该问题就是丁烷上的二取代问题,由定一移一得共有9种,其中核磁共振氢谱显示有3组峰,且峰面积之比为![]() 的结构简式为
的结构简式为![]() ;
;
(7)根据逆推法,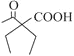 可由
可由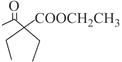 水解制得,对比碳骨架和反应⑤,
水解制得,对比碳骨架和反应⑤,![]() 可制备
可制备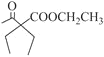 ,最后依据信息②,即可得到正确的合成路线:
,最后依据信息②,即可得到正确的合成路线:![]()
![]()
![]()
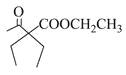
![]()
 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室制备 1,2二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O CH2=CH2+Br2―→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2―→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量溴和足量的乙醇 制备1,2-二溴乙烷的装置如下图所示:
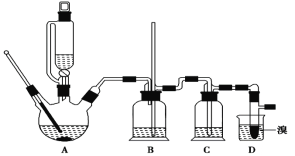
有关数据列表如下:
乙醇 | 1 ,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0 .79 | 2.2 | 0 .71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_________。(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 C 中应加入________,其目的是吸收反应中可能生成的酸性气体。(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断 1,2-二溴乙烷制备反应已经结束的最简单方法是_________________________。
(4)将 1,2 二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________________层(填“上”、“下”)。
(5)若产物中有少量未反应的 Br2,最好用___________洗涤除去。(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用_____的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下图,

下列说法正确的是( )
A. 313K时,根据曲线计算可知Ksp(SrSO4) 数量级为10-5
B. 三个不同温度中,313 K时Ksp(SrSO4)最大
C. 283 K时,图中a点对应的溶液是饱和溶液
D. 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
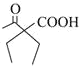
【题目】福酚美克是一种影响机体免疫功能的药物,可通过以下方法合成:
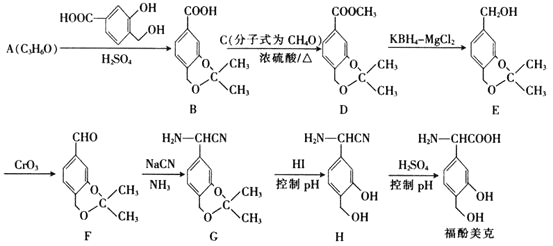
已知:
①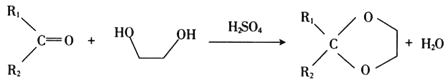 ;
;
②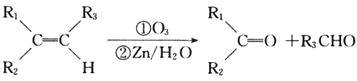 。
。
(1)C的名称为________,A的结构简式为________________。
(2)福酚美克中所含官能团有________________![]() 填名称
填名称![]() 。
。![]() 的反应类型为________。
的反应类型为________。
(3)已知![]() 的转化属于取代反应,则该反应的另一产物的结构简式为________。
的转化属于取代反应,则该反应的另一产物的结构简式为________。
(4)写出F发生银镜反应的化学方程式:________________________________。
(5)E的一种同分异构体Q满足下列条件,则Q的结构简式为________。
①Q的苯环上只有2个取代基,且Q的核磁共振氢谱图中有4组吸收峰
②Q能与![]() 溶液发生显色反应
溶液发生显色反应
③![]() 最多能与
最多能与![]() 发生反应
发生反应
(6)根据已有知识并结合题给信息,写出以![]() 为原料
为原料![]() 无机试剂任用
无机试剂任用![]() 制备
制备 的合成路线流程图_________
的合成路线流程图_________![]() 无机试剂任选
无机试剂任选![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铅蓄电池为电源,石墨为电极电解CuSO4溶液(足量),装置如下图。若一段时间后Y电极上有6.4 g红色物质析出,停止电解。下列说法正确的是( )
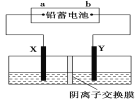
A.a为铅蓄电池的负极
B.电解过程中SO42-向右侧移动
C.电解结束时,左侧溶液质量增重8 g
D.铅蓄电池工作时正极电极反应式为:PbSO4+2e-===Pb+SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,![]() 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:![]()
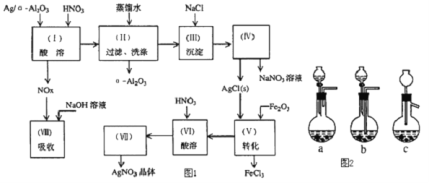
阅读上述实验流程,完成下列填空:
![]() 加酸溶解应该选用装置
加酸溶解应该选用装置![]() 图
图![]() ______
______ ![]() 选填a、b、
选填a、b、![]() .
.
![]() 在实验操作
在实验操作![]() Ⅱ
Ⅱ![]() ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
![]() 实验操作
实验操作![]() Ⅳ
Ⅳ![]() 所需玻璃仪器为 ______
所需玻璃仪器为 ______ ![]() 填写三种
填写三种![]() .
.
![]() 实验操作
实验操作![]() Ⅶ
Ⅶ![]() 从
从![]() 溶液获得
溶液获得![]() 晶体需要进行的实验操作依次为: ______
晶体需要进行的实验操作依次为: ______ ![]() 多选扣分
多选扣分![]() .
.
![]() 蒸馏
蒸馏![]() 蒸发
蒸发![]() 灼烧
灼烧![]() 冷却结晶
冷却结晶
![]() 已知:
已知:![]() ;
;
![]()
NO和![]() 的混合气体的组成可表示为
的混合气体的组成可表示为![]() 该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
![]()
![]()
![]()
![]() 已知
已知![]() 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
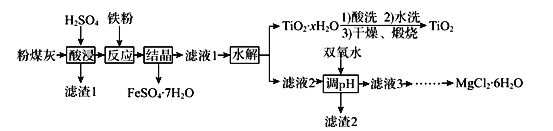
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO42-和一种阳离子
②常温下,Ksp[Al(OH)3]=1.0×10-34,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mg(OH)2]= 5.61×10-12
③滤液1中仍有Fe2+剩余
请回答下列问题:
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有_______________________
(2)“水解”反应的离子方程式为______________________________________。怎样判断TiO2xH2O沉淀已经洗涤干净____________________________________________。
(3)加入双氧水调节溶液pH时离子方程式为_______________________________________。滤渣2成分为________________。为使滤渣2沉淀完全(溶液中离子浓度小于10-5mol/L)。需“调pH”为________。(保留两位有效数字)
(4)滤液3在蒸发结晶制备MgCl26H2O应注意_____________________________________。
(5)“结晶”需控制在70℃左右,温度过高的后果会导致的后果为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当电池工作时,下列说法错误的

A. 甲池中N极的电极反应式为:O2+4e-+4H+=2H2O
B. 当N极消耗5.6L(标准状况下)O2时,铁极增重32g
C. 电子的流动方向为M→Fe→CuSO4溶液→Cu→N
D. M极上发生的是氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com