
科技工作者提出用铝粉处理含亚硝酸盐废水的思路:调节亚硝酸盐废水酸碱性,使其pH>12,然后加入适量的铝粉、搅拌,生成可进入大气循环的气体,从而实现预期目的。下列判断错误的是
A.处理过程中,PH减小 B.废水处理中,亚硝酸盐被还原
C.废水处理时铝单质转化为AlO2- D.铝粉颗粒大小影响废水处理的速率
科目:高中化学 来源:2015-2016学年吉林省高二上期中考试化学试卷(解析版) 题型:选择题
下列混合溶液中,各离子浓度的大小顺序正确的是
A.10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合:
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.10 mL0.1mol/LNH4Cl溶液与5 mL0.2mol/LNaOH溶液混合:
c(Na+)= c(Cl-)>c(OH-)>c(H+)
C.10mL0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合:
(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合:
c(Cl-)> c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第二次月考化学试卷(解析版) 题型:选择题
有体积相同的两份营养液,其配方如下:
KCl | K2SO4 | ZnSO4 | ZnCl2 | |
第一份 | 0.3 mol | 0.2 mol | 0.1 mol | —— |
第二份 | 0.1 mol | 0.3 mol | —— | 0.1 mol |
两份营养液中各离子浓度
A.完全不同 B.完全相同 C.仅c(K+)相同 D.仅c(Cl-)相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
下列关于弱电解质的说法中,正确的是
A.弱电解质需要通电才能发生电离
B.醋酸达到电离平衡时,不存在:CH3COO-+H+ CH3COOH
CH3COOH
C.H2SO4是共价化合物,所以它是弱电解质
D.电离平衡右移,电解质分子的浓度不一定减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上10月月考化学试卷(解析版) 题型:选择题
恒温恒压下,一个容积可变的密闭容器中发生反应:A(g)+B(g) C(g)。若开始时通入1mol A 和1mol B,则达到平衡时生成a molC.则下列说法错误的是
C(g)。若开始时通入1mol A 和1mol B,则达到平衡时生成a molC.则下列说法错误的是
A.若开始时通入3mol A 和3mol B,则达到平衡时,生成C的物质的量为3a mol
B.若开始时通入4mol A 和4mol B、2molC,则达到平衡时,生成B的物质的量一定大于4 mol
C.若开始时通入2mol A 和2mol B、1mol C,则达到平衡时,在通入3 mol C,则再次达到平衡后,C的体积分数为a /(2-a)
D.若在原平衡体系中,在通入1mol A 和1mol B,则混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期第二次月考理综化学试卷(解析版) 题型:选择题
以下数值大于或等于阿伏加德罗常数的是
A.6g石墨中的共价键数目
B.常温常压下,17g ND3中所含分子数目
C.向0.2mol NH4Al(SO4)2溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目
D.0.1mol羟基(—OH)中所含电子数目
查看答案和解析>>
科目:高中化学 来源:名师精品推荐(解析版) 题型:?????
将50g溶质质量分数为20%的烧碱溶液稀释为10%,下列说法错误的是
A.向其中加入50g蒸馏水
B.操作步骤是计算、量取、混匀、装瓶贴标签
C.必须使用的玻璃仪器是烧杯、量筒、玻璃棒
D.若量取水时俯视读数,所配溶液的溶质质量分数偏大
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省牡丹江市高三9月月考化学试卷(解析版) 题型:填空题
(10分)元素X、Y、Z、W、M、N原子序数依次增大。X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期。它们四者原子序数之和为22,最外层电子数之和为16。在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构。请回答下列问题:
(1)M元素在周期表中的位置是 ,X、Y、Z、W、M的原子半径由大到小的顺序为 (用元素符号表示)。
(2)写出Y2X2的电子式 ;Z2X4结构式 。
(3)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味,且能使品红溶液褪色的气体放出,该反应的离子方程式为 。
(4)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式 。
(5)写出足量NW2通入硝酸钡溶液中的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:填空题
(10分)某研究小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱(Na2CO3)和氯化铵(NH4Cl)。
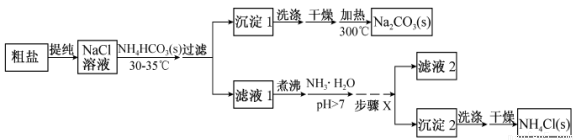
已知盐的热分解温度:NH4HCO3 36℃;NaHCO3 270℃;NH4Cl 340℃;Na2CO3>850℃
请回答:
(1)从NaCl溶液到沉淀1的过程中,需蒸发浓缩。在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3固体之后,其原因是 。
(2)为提高NH4Cl产品的产率和纯度,需在滤液1中加入氨水,理由是 ;步骤X包括的操作有 。
(3)测定NH4Cl产品的纯度时,可采用的方法:在NH4Cl溶液中加入甲醛使之生成游离酸(4NH4Cl+6HCHO=(CH2)6N4+4HCl+6H2O),然后以酚酞为指示剂,用NaOH标准溶液(需用邻苯二甲酸氢钾基准物标定)进行滴定。
①下列有关说法正确的是 。
A.为了减少滴定误差,滴定管、锥形瓶均须用待装液润洗
B.标准NaOH溶液可以装入带有耐腐蚀旋塞的玻璃滴定管中
C.开始滴定前,不需擦去滴定管尖悬挂的液滴
D.三次平行测定时,每次需将滴定管中的液面调至“0”刻度或“0”刻度以下的附近位置
②若用来标定NaOH标准溶液的邻苯二甲酸氢钾基准物使用前未烘至恒重,则测得NH4Cl产品的含量比实际含量 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com