
【题目】一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物 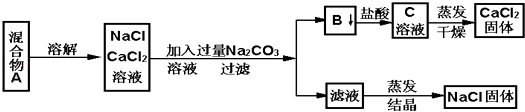 填空和回答下列问题
填空和回答下列问题
(1)B物质是(写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 .
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 .
科目:高中化学 来源: 题型:
【题目】草酸(化学式为H2C2O4 , 是一种二元酸)存在于自然界的植物中.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是有气泡冒出且澄清石灰水变浑浊,由此可知草酸晶体分解的产物中有 . 装置B的主要作用是冷凝(水蒸气和草酸),防止草酸进入装置C中发生反应(填化学方程式),干扰分解生成气体的检验.
(2)乙组同学认为草酸晶体分解的产物中还可能含有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置进行实验.
①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G、H、D、I.其中装置F中发生的化学反应为 . 两次使用了D装置,其中第一个D装置的作用是 , 装置H反应管中盛有的物质是 .
②能证明草酸晶体分解产物中有CO的现象是H中物质变为色;且 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在指定的环境中一定能大量共存的是( )
A.常温下,在c(H+)/c(OH﹣)=1×1012的溶液中:I﹣、Cl﹣、NO ![]() 、Na+
、Na+
B.在能使石蕊变红色的溶液中:Na+、S2﹣、SO ![]() 、CO
、CO ![]()
C.在加入铝粉能产生H2的溶液中:NH ![]() 、Na+、NO
、Na+、NO ![]() 、Cl﹣
、Cl﹣
D.常温下由水电离出的c(H+)=1×10﹣12 mol?L﹣1的溶液中:K+、Cl﹣、NO ![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484KJ热量,下列热化学方程式正确的是( )
A.H2(g)+ ![]() ?O2(g)═H2O(g)△H=+242 kJ/mol
?O2(g)═H2O(g)△H=+242 kJ/mol
B.2H2(g)+O2(g)═2H2O(l)△H=﹣484kJ/mol
C.H2(g)+ ![]() ?O2(g)═H2O(g)△H=﹣242kJ/mol
?O2(g)═H2O(g)△H=﹣242kJ/mol
D.2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K= ![]() .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2OCO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量在化学中占有重要地位,请回答下列问题:
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为M gmol﹣1 . 若阿伏加德罗常数用NA表示,则:
①该气体所含原子总数为 个;(用含有NA的式子表示)
②该气体溶于水(不考虑与水反应)后形成V L溶液,其溶液的物质的量浓度为
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(3)某盐混合溶液中含有Na+、Mg2+、Cl﹣、SO42﹣ , 测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol
L﹣1、0.25molL﹣1、0.4molL﹣1 , 则c(SO42﹣)=
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某人设想利用①3FeCl2+4H2O ![]() Fe3O4+6HCl+H2②Fe3O4+
Fe3O4+6HCl+H2②Fe3O4+ ![]() Cl2+6HCl
Cl2+6HCl ![]() 3FeCl3+3H2O+
3FeCl3+3H2O+ ![]() O2 ③3FeCl3
O2 ③3FeCl3 ![]() 3FeCl2+
3FeCl2+ ![]() Cl2 这三个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是( )
Cl2 这三个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是( )
A.O2
B.Cl2
C.HCl
D.H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭的2L容器中装有4mol SO2和2mol O2 , 在一定条件下开始反应2SO2(g)+O2(g)2SO3(g).2min末测得容器中有1.6mol SO2 , 请计算:
(1)2min末SO3的浓度;
(2)2min内SO2的平均反应速率.
(3)2min末SO2的转化率.
(4)反应前后的压强之比.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com