
【题目】已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484KJ热量,下列热化学方程式正确的是( )
A.H2(g)+ ![]() ?O2(g)═H2O(g)△H=+242 kJ/mol
?O2(g)═H2O(g)△H=+242 kJ/mol
B.2H2(g)+O2(g)═2H2O(l)△H=﹣484kJ/mol
C.H2(g)+ ![]() ?O2(g)═H2O(g)△H=﹣242kJ/mol
?O2(g)═H2O(g)△H=﹣242kJ/mol
D.2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol
【答案】C
【解析】解:A、放热而不是吸热,所以1mol氢气燃烧生成水蒸气放出242kJ热量,所以H2(g)+ ![]() O2(g)═H2O(g)△H=﹣242kJ/mol,故A错误; B、是生成水蒸气,而不是液态水,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=﹣484kJ/mol,故B错误;
O2(g)═H2O(g)△H=﹣242kJ/mol,故A错误; B、是生成水蒸气,而不是液态水,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=﹣484kJ/mol,故B错误;
C、2mol氢气燃烧生成水蒸气放出484kJ热量,则1mol氢气燃烧生成水蒸气放出242kJ热量,所以H2(g)+ ![]() O2(g)═H2O(g)△H=﹣242kJ/mol,故C正确;
O2(g)═H2O(g)△H=﹣242kJ/mol,故C正确;
D、2mol氢气燃烧生成水蒸气放出484kJ热量,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=﹣484kJ/mol,故D错误;
故选C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】室温下,将碳酸钠溶液加热至70℃,其结果是( )
A.溶液中c(CO32﹣)增大
B.水的电离程序不变
C.KW(水的离子积)将变小
D.溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化铝和氢氧化铝的说法正确的是( )
A. 氧化铝是一种比较好的耐火材料,可用来制造耐火坩埚
B. 氧化铝是典型的两性氧化物,可与氨水反应生成四羟基合铝酸盐
C. 因为氢氧化铝受热易分解,所以具有两性
D. 两性氢氧化物只能与强酸、强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是( )
A.v(B2)=0.8 mol/(Ls)
B.v(A2)=0.5 mol/(Ls)
C.v(C)=0.9 mol/(Ls)
D.v(B2)=1.2 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲曲线表示在最适温度下,某种酶促反应速率与反应物浓度之间的关系。其余两条曲线分别表示该酶促反应的反应速率受温度和pH的影响情况。回答下列问题:

(1)甲曲线中,若在A点适当提高温度,反应速率将会_____________________;在B点适当增加酶的浓度,反应速率将会__________________。
(2)丙曲线中,H点代表该酶的_____________________。
(3)若想要短期保存该酶,应选择曲线中的________点所对应的温度。
(4)探究温度对酶活性的影响时,通常选择_________________________(填“淀粉酶”或“过氧化氢酶”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物 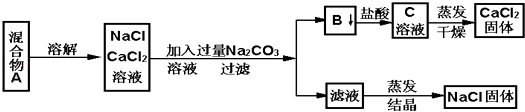 填空和回答下列问题
填空和回答下列问题
(1)B物质是(写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 .
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一些建筑工地的食堂中,常发生将工业用盐当作食用盐而引起中毒的现象.该盐的化学式为( )
A. MgCl2B. KClC. NaNO2D. MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碰撞理论是一种较直观的反应速率理论,下列有关碰撞理论叙述正确的是
A.反应物分子必须碰撞才有可能发生反应
B.发生有效碰撞的分子具有最高的能量
C.有效碰撞是活化分子在一定方向上的碰撞
D.活化分子的平均能量称之活化能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com