
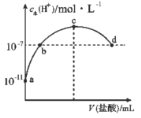
【题目】常温下,向![]() 氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是
氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是
A.a点溶液中![]()
B.b、d两点溶液均呈中性
C.c点溶液中![]()
D.a、b之间的点可能满足:![]()
【答案】D
【解析】
A.a点为NH3H2O,在溶液中存在NH3H2O和水的电离平移,则c(NH3H2O)>c(OH-)>c(NH4+)>c(H+),故A错误;
B.c点水的电离程度最大,说明c点恰好完全反应生成NH4Cl,NH4+水解促进水的电离,NH4Cl为强酸弱碱盐显酸性,继续加稀盐酸,则d点一定显酸性,故B错误;
C.c点水的电离程度最大,说明c点恰好完全反应生成NH4Cl,NH4+水解促进水的电离,NH4Cl为强酸弱碱盐显酸性,即c(H+)>c(OH-),故C错误;
D.a、b之间的任意一点,溶液都呈碱性,则c(H+)<c(OH-),c(NH4+)>c(Cl-),即存在c(NH4+)>c(Cl-)>c(H+)<c(OH-),故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7个横行,每一个横行称为“周期”,周期序数=电子层数;元素周期表共有18列,每一列称为 “族”,下表中的7列为主族元素,分别用罗马数字Ⅰ、Ⅱ、……表明族序数,族序数=最外层电子数。
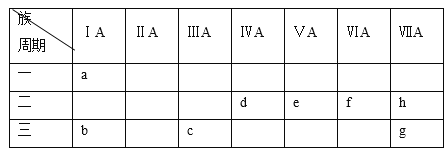
根据a~h各元素的性质,选择相应的化学符号、化学式或化学方程式填空:
(1)单质氧化性最强的是__________,酸性最强的含氧酸是_____________。
(2)写出e的碱性气态氢化物的电子式_____,将它和化合物df 2通入饱和食盐水发生反应的化学方程式是_____。
(3)最高价氧化物对应的水化物中,碱性最强的是___________。
(4)在b、c、g、h中,常见离子半径最大的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
CaS(s)+4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是__________。
A.  B.
B. 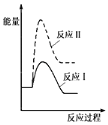
C. 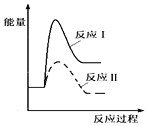 D.
D.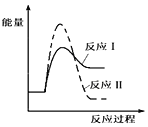
(2)在温度、容积相同且不变的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下表(已知2SO2(g)+O2(g) ![]() 2SO3(g)△H=196.6kJ·mol-1) 则:
2SO3(g)△H=196.6kJ·mol-1) 则:
容器 | 甲 | 乙 | 丙 | (填>,=,<) A.2c1_____c3 B.a+b_____196.6 C.2p2____p3 D.α1+α3___1 |
反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO3 | |
SO3的浓度 (mol·L-1) | C1 | C2 | C3 | |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ | |
体系压强 | P1 | P2 | P3 | |
反应物转化率 | α1 | α2 | α3 |
(3)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入氨水中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。
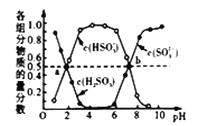
请写出a点时n(HSO3-):n(H2SO3)=______,b点时溶液pH=7,则n(NH4+):n(HSO3-)=_____。
(4)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO ![]() 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图所示:
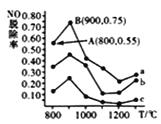
①曲线c对应NH3与NO的物质的量之比是__________。
②曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为__________mg/(m3·s)。
(5)已知Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9,向0.4mol/L Na2SO4的溶液中加入足量BaCO3粉末(忽略体积变化),充分搅拌,发生反应SO42- (aq)+BaCO3(s) ![]() BaSO4 (s)+CO32-(aq) 静置后沉淀转化达到平衡。此时溶液中的c(SO42-)=____mol·L-1(保留小数点后两位).
BaSO4 (s)+CO32-(aq) 静置后沉淀转化达到平衡。此时溶液中的c(SO42-)=____mol·L-1(保留小数点后两位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.分子式为C8H8O2的芳香族化合物中属于羧酸的同分异构体有3种
B.分子式为C4H8BrCl的有机物共有9种
C.等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的体积相同
)完全燃烧,消耗氧气的体积相同
D.分子式为C4H8Cl2且含有两个甲基的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
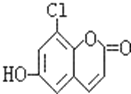
A.2molBr2、2molNaOHB.3molBr2、4molNaOH
C.3molBr2、5molNaOHD.4molBr2、5molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物2苯基丙烯(![]() ),下列说法正确的是
),下列说法正确的是
A. 不能使稀高锰酸钾溶液褪色
B. 可以发生加成聚合反应
C. 分子中所有原子共平面
D. 易溶于水及甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最内层电子数是最外层电子数的1/3,下列说法中正确的是
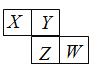
A.Y、Z元素的最高正价均为+6价
B.X、Y元素形成的化合物均为酸性氧化物
C.最高价氧化物对应水化物的酸性:W>Z
D.W单质能与氢氧化钠溶液反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加,由这些元素组成的常见物质的转化关系如下图,其中a、b、d、g为化合物,a为淡黄色固体,c是Z的单质,该单质与沸水缓慢反应,且该单质可制造照明弹;f为固体单质。下列有关说法正确的是
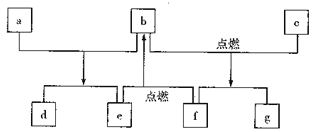
A. 简单离子的半径:Y>Z>X B. 元素的非金属性:W>X
C. 最高价氧化物对应水化物的碱性:Y>Z D. X、Y两种元素组成的化合物只含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)为原料制取红矾钠 (Na2Cr2O7·2H2O)的流程如图所示。
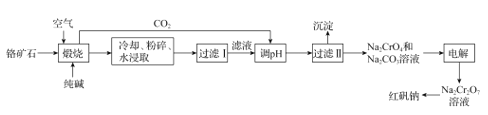
已知:I.Cr2O3在碱性条件下易被氧化;
II.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3 +Na2CO3=2NaAlO2 +CO2↑;
III.2CrO42-+2H+![]() Cr2O72- +H2O K=1.0×1012
Cr2O72- +H2O K=1.0×1012
(1)“煅烧”时,Cr2O3参加反应的化学方程式为_____。若“煅烧”操作最适宜的温度是800~900℃,则在实验室中进行此项操作时,应选择_____坩埚(填字母)。
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有_____(填化学式)。
(3)“过滤II”所得沉淀主要有______(填化学式)。
(4)由Na2Cr2O7溶液制备红矾钠的具体实验操作有_____,经洗涤、干燥得到红矾钠样品。
(5)“电解”时,利用以下装置将Na2CrO4溶液转化为Na2Cr2O7溶液,当a、b均为石墨电极时,a电极的电极反应式为____。若初始加入电解池中的c (Na2CrO4)=1.0mol·L-l,随着“电解”的进行,当溶液pH=6时,Na2CrO4的转化率为______(忽略电解过程中溶液体积变化)。
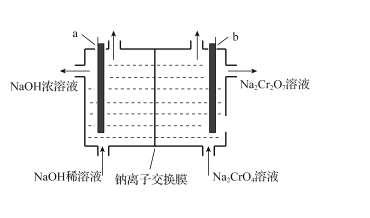
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com