
����Ŀ����A��һ����Ҫ�Ļ���ԭ�ϣ���������·�ߺϳ�X��
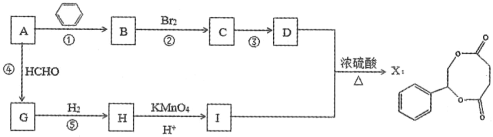
��֪��RC��CH��HCHO![]() RC��CCH2OH
RC��CCH2OH
��ش��������⣺
(1)����Ӧ�١��ڡ��ܵ�ԭ�������ʾ�Ϊ100%����A������Ϊ��________��
(2)����G�Ľṹ��ʽΪ��_________��
(3)д����Ӧ�۵Ļ�ѧ��Ӧ����ʽ��_________��
(4)����E��D�����������ɵ��л����E�ܷ���������Ӧ��д��E�й��������ƣ�________��
(5)����H������I������һ�������ºϳ���״�ۺ����д����ѧ����ʽ��______��
(6)��������������D��ͬ���칹�干��_______�֣�д������һ�ֵĽṹ��ʽ_____��
i.��FeCl3��Һ�ܷ�����ɫ��Ӧ ii.�����ϵ�һ�ȴ���ֻ��һ��
���𰸡���Ȳ HOCH2C��CCH2OH ![]() +2NaOH
+2NaOH![]()
![]() +2NaBr �ʻ���ȩ�� nHOCH2CH2CH2CH2OH+nHOOCCH2CH2COOH
+2NaBr �ʻ���ȩ�� nHOCH2CH2CH2CH2OH+nHOOCCH2CH2COOH![]()
![]() +(2n-1)H2O 6
+(2n-1)H2O 6 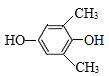
��������
����X�ṹ��ʽ��֪��D��I����������Ӧ����X��H����������Ӧ����I����IΪ�ᣬ��X��֪IΪHOOCCH2CH2COOH��DΪ![]() ��B���巢���ӳɷ�Ӧ����C��C�к�����ԭ�ӣ�C����ˮ�ⷴӦ����D����CΪ
��B���巢���ӳɷ�Ӧ����C��C�к�����ԭ�ӣ�C����ˮ�ⷴӦ����D����CΪ![]() ��BΪ
��BΪ![]() ������Ӧ�١��ڡ��ܵ�ԭ�������ʾ�Ϊ100%��A�ͱ������ӳɷ�Ӧ����B����AΪHC��CH��������Ϣ֪GΪHOCH2C��CCH2OH��G�����������ӳɷ�Ӧ����HΪHOCH2CH2CH2CH2OH�������Ŀ�������
������Ӧ�١��ڡ��ܵ�ԭ�������ʾ�Ϊ100%��A�ͱ������ӳɷ�Ӧ����B����AΪHC��CH��������Ϣ֪GΪHOCH2C��CCH2OH��G�����������ӳɷ�Ӧ����HΪHOCH2CH2CH2CH2OH�������Ŀ�������
��������������֪��A��HC��CH��B��![]() ��C��
��C��![]() ��D��
��D��![]() ��G��HOCH2C��CCH2OH��H��HOCH2CH2CH2CH2OH��I��HOOCCH2CH2COOH��
��G��HOCH2C��CCH2OH��H��HOCH2CH2CH2CH2OH��I��HOOCCH2CH2COOH��
(1)������������֪����AΪHC��CH��A������Ϊ����Ȳ��
(2)������������֪������G�Ľṹ��ʽΪ��HOCH2C��CCH2OH��
(3)C��![]() ������Brԭ�ӣ���NaOH��ˮ��Һ���ȣ�����ȡ����Ӧ����D��
������Brԭ�ӣ���NaOH��ˮ��Һ���ȣ�����ȡ����Ӧ����D��![]() ����Ӧ�۵Ļ�ѧ��Ӧ����ʽ��
����Ӧ�۵Ļ�ѧ��Ӧ����ʽ��![]() +2NaOH
+2NaOH![]()
![]() +2NaBr��
+2NaBr��
(4) D��![]() ��D��u������������E�����ǻ���������Ϊ�ʻ���ȩ������EΪ
��D��u������������E�����ǻ���������Ϊ�ʻ���ȩ������EΪ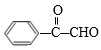 ��
��
(5)H��HOCH2CH2CH2CH2OH��I��HOOCCH2CH2COOH������H������I������һ�������·������۷�Ӧ�ϳ���״�ۺ����ѧ����ʽΪ��nHOCH2CH2CH2CH2OH+nHOOCCH2CH2COOH![]()
![]() +(2n-1)H2O��
+(2n-1)H2O��
(6)DΪ![]() ��D��ͬ���칹����ϣ�������FeCl3��Һ�ܷ�����ɫ��Ӧ��˵�����з��ǻ������������ϵ�һ�ȴ���ֻ��һ�֣�˵��������ֻ��һ��Hԭ�ӣ������������ͬ���칹���У�Ӧ�ú����������ǻ�����������
��D��ͬ���칹����ϣ�������FeCl3��Һ�ܷ�����ɫ��Ӧ��˵�����з��ǻ������������ϵ�һ�ȴ���ֻ��һ�֣�˵��������ֻ��һ��Hԭ�ӣ������������ͬ���칹���У�Ӧ�ú����������ǻ�����������
������������ڣ��������ǻ�������Ի������ҽṹ�Գƣ���2�֣�
�����������䣬�������ǻ���ԣ���1�֣�
�����������ԣ��������ǻ��������ڻ�����ҽṹ�Գƣ���3�֣�
����������Ľṹ��6�֣�
���е�һ��ͬ���칹��ṹ��ʽΪ ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3 mol A��1 mol B�����һ����ɱ���ܱ�����P�У��Դ�ʱ���¶ȡ�ѹǿ�������Ϊ��ʼ�������������·�Ӧ��
3A(g)��B(g) ![]() 2C(g)��D(g)���ﵽƽ��ʱC��Ũ��Ϊw mol/L���ش��������⣺
2C(g)��D(g)���ﵽƽ��ʱC��Ũ��Ϊw mol/L���ش��������⣺
(1)�����¶Ⱥ�ѹǿ���䣬������������ȳ�������P���й����ʣ�ƽ���C��Ũ����Ϊw mol/L����_____��
A��6 mol A��2 mol B B��3 mol A��1 mol B��2 mol C
C��2 mol C��1 mol B��1 mol D D��1 mol C��2 mol D
(2)����ԭ��ʼ�¶Ⱥ�������䣬Ҫʹƽ���C��Ũ����Ϊw mol/L��Ӧ�������������������Q�г����й�����_____��
A��3 mol A��1 mol B B��4 mol C��2 mol D
C��1.5 mol A��0.5 mol B��1 mol C��0.5 mol D D�����ж�
(3)����ԭ��ʼ�¶Ⱥ�������䣬����3 mol A��1 mol B���������Q�з�����Ӧ����ƽ��ʱC��Ũ�Ⱥ�w mol/L�Ĺ�ϵ��____��
A������w mol/L B��С��w mol/L C������w mol/L D�����Ƚ�
(4)��2 mol C��2 mol D����ʼ�¶Ⱥ�ѹǿ��������Q�У������¶Ⱥ�������䣬ƽ��ʱC��Ũ��Ϊv mol/L����v��w�Ĺ�ϵ��_____��
A��v>w B��v<w C��v��w D�����Ƚ�
(5)ά��ԭ��ʼ�¶Ⱥ�������䣬������������ȳ�������Q��ʹƽ��ʱC��Ũ��Ϊv mol/L ____��
A��1 mol C��0.5 mol D B��3 mol A��2 mol B
C��3 mol A��1 mol B��1 mol D D�����Ͼ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��H2SO3�ĵ��볣��K1=1.3��10-2��K2=6.2��10-8����amolL-1NaHSO3��Һ��bmolL-1NaOH��Һ��������(a>0��b>0)�����������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A.a=bʱ��c(OH-)=c(H+)+c(HSO3-)
B.a=3bʱ��c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
C.����ҺpH=7ʱ��c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.��4c(Na+)=5c(SO32-)+5c(HSO3-)+5c(H2SO3)����a=4b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A�ǻ����л�����ԭ�ϣ���A�Ʊ��߷���E��ҽҩ�м���K�ĺϳ�·�ߣ����ַ�Ӧ������ȥ������ͼ��ʾ��
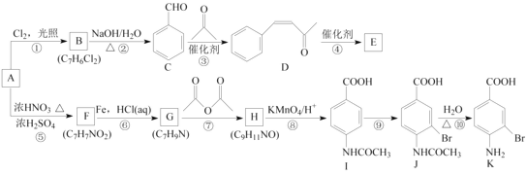
��֪����![]() ��
��
��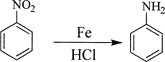
�ش��������⣺
��1��A��������________��I���й����ŵ�������________��
��2����Ӧ�ߵ�������________����ķ�Ӧ������________��
��3��д����Ӧ�ڵĻ�ѧ����ʽ��____________________________________________________��
��4��D�����������________��ԭ�ӹ�ƽ�档E�Ľṹ��ʽΪ________��
��5��д��һ��ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ��________��
�ٱ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ�
�ڼ�����������Һ��Ӧ������NaOH��Һ��Ӧ��
��6������DΪ��ʼԭ���Ʊ�![]() �ĺϳ�·�߲���������
�ĺϳ�·�߲���������
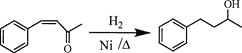 ________�����Լ����ܼ���ѡ����
________�����Լ����ܼ���ѡ����
�ϳ�·������ͼʾ�����£�
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ס��ҡ�����X��4����ѧ��ѧ�г��������ʣ���ת����ϵ������ͼ�����X��Ҫ���X�ܻ�������������
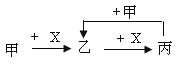
A.C��O2B.SO2 ��NaOH��Һ
C.Cl2��FeD.AlCl3��Һ��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ࡢ��֬�������ʶ���������ϢϢ��ص����ʣ������й�˵����ȷ����![]()
![]()
A.�����Ǻ�������ͬϵ����ۺ���ά����ͬ���칹��
B.���ۡ���ά�ء���֬�������ʶ��Ǹ߷��ӻ�������ܷ���ˮ�ⷴӦ
C.�����ϵ���˿����������ɻ���ʼ�����е���˿���������ֱ�����ά�غ���֬
D.ͨ������ʱ��������ζ���Լ����˿����ɴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɸ߷��ӽ����������ϼ��ķ�Ӧ��
 +(2n-1)H2O
+(2n-1)H2O
����˵������ȷ����
A.�ۺ���Ӧ������������ʣ���NaOH�����ڽӴ�
B.�ۺ���ĺϳɷ�ӦΪ���۷�Ӧ
C.1mol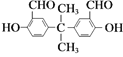 ������������Һ���ÿ�����2mol��
������������Һ���ÿ�����2mol��
D.ͨ�������ⶨ��ƽ����Է����������ɵ���ۺ϶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ������з�����Ӧ��![]() ������ӦΪ���ȷ�Ӧ��H2O��H2�����ʵ�����ʱ��ı仯��ͼ��ʾ��2minʱ���ı�һ����������ı�������ǣ� ��
������ӦΪ���ȷ�Ӧ��H2O��H2�����ʵ�����ʱ��ı仯��ͼ��ʾ��2minʱ���ı�һ����������ı�������ǣ� ��
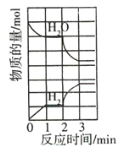
A.��Сn(H2O)B.����n(H2)
C.����ѹǿ����С���������D.�����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2CO3��Һ�����ᷴӦ�����е������仯��ͼ��ʾ������ѡ�������ǣ� ��

A.CO2(g)+H2O(l)=H2CO3(aq)�Ƿ��ȷ�Ӧ
B.CO32-(aq)+2H+(aq)=CO2(g)+H2O(l)�Ƿ��ȷ�Ӧ
C.HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)�Ƿ��ȷ�Ӧ
D.HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com