
【题目】下列物质存放方法错误的是( )
A.铝片长期放置在不密封的纸盒里B.烧碱长期放置在烧杯中
C.铁粉密封在试剂瓶中D.白磷存放于冷水中
科目:高中化学 来源: 题型:
【题目】把aL含(NH4)2SO4和NH4NO3的混和溶液分成两等份,一份加入b mol的烧碱并加热,恰好将全部NH4+转变成NH3放出;另一份需含c mol 的BaCl2溶液恰能完全沉淀SO42-,则原溶液中NO3-的物质的的浓度是( )
A. (2b-4c)/a mol/L B. (b-2c)/a mol/L
C. (2b-c)/amol/L D. (b-4c)/a mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是( )
①2Fe3++2I-===2Fe2++I2
②2Fe2++Cl2===2Fe3++2Cl-
③2MnO![]() +10Cl-+16H+===2Mn2++5Cl2↑+8H2O
+10Cl-+16H+===2Mn2++5Cl2↑+8H2O
A.Fe3+>Cl2>MnO![]() B.Fe3+>Cl2>I2 C.I2>Cl2>Fe3+ D.MnO
B.Fe3+>Cl2>I2 C.I2>Cl2>Fe3+ D.MnO![]() >Cl2>Fe3+
>Cl2>Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HNO2的电离平衡常数为K=4.6×10﹣4(已知 ![]() =2.14),向20mL0.01molL﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
=2.14),向20mL0.01molL﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( ) 
A.HNO2的电离方程式为HNO2=NO2﹣+H+
B.a点H2O电离出的c(H+)=2.14×10﹣3molL﹣1
C.b点溶液中离子浓度大小关系为c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣)
D.X值等于20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究CH3COOH、HA和MOH的酸碱性的相对强弱,某兴趣小组设计了以下实验:室温下,将pH=2的两种酸溶液CH3COOH、HA和pH=12的碱MOH溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图1所示,根据所给数据,请回答下列问题: 
(1)HA为酸 (填“强”或“弱”).稀释后 HA溶液中水电离出来的 c(H+)醋酸溶液中水电离出来c(H+)(填“大于”、“等于”或“小于”).
若b+c=14,则MOH为碱(填“强”或“弱”).
(2)常温下0.10mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变大的是 .
A.c(H+)
B.c(H+)/c(CH3COOH)
C.c(H+)c(OH﹣)
D.c(OH﹣)/(H+)
(3)常温下,用0.10molL﹣1 NaOH溶液分别滴定20mL 0.10molL﹣1 HCl溶液和20mL 0.10 molL﹣1 CH3COOH溶液,得到两条滴定曲线,如图所示.如图中滴定醋酸溶液的曲线是(填“图2”或“图3”);曲线上E点pH>8的原因是(用离子方程式表示) .
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中离子浓度由大到小顺序为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480mL含NaClO25%,密度为1.19g/cm3的消毒液.下列说法正确的是
A. 配制过程只需要三种仪器即可完成
B. 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C. 定容时俯视容量瓶的刻度线,会造成所配溶液物质的量浓度偏低
D. 需用托盘天平称量的NaClO固体的质量为148.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸(H2FeCO4)是一种多功能、高效无毒的新型绿色水处理剂,投入水中会迅速发生反应。
(1)Na2FeO4中Fe的化合价为。.
(2)已知:常温下高铁酸为紫黑色固体,将H2FeO4投入水中,有气体生成,同时有红褐色沉淀产生,则H2FeO4与水反应的化学方程式为。
(3)在工业上制备Na2FeO4的方法有多种。
Ⅰ.干法制备的反应原理如下:
2FeSO4+6Na2O2=aNa2FeO4+M↑+2Na2O+2Na2SO4
①a=。
②每生成1mol M,该反应转移电子的物质的量为mol。
Ⅱ.湿法制备的工艺流程如下: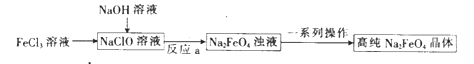
己知:Na2FeO4在强碱性溶液中的溶解度较小。
③反应a中,生成物除了Na2FeO4外,另一种盐的化学式为 。
④一系列操作包括过滤、、。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述 ![]() 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )
A.最多有6个碳原子在一条直线上
B.该烃属于苯的同系物
C.至少有10个碳原子在同一平面上
D.所有碳原子不可能都在同一平面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com