
【题目】下列说法正确的是( )
A.生石灰与水混合的过程只发生物理变化
B.O3是由3个氧原子构成的化合物
C.CuSO4·5H2O是一种混合物
D.可用丁达尔效应区分溶液与胶体
科目:高中化学 来源: 题型:
【题目】一定质量的铝片分别和相同浓度、相同体积氢氧化钠溶液和盐酸反应,放出氢气的质量
A.一样多B.和盐酸反应放出的多
C.和氢氧化钠溶液反应放出的多D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:S+2KNO3+3C=K2S+N2↑+3CO2↑,该反应的还原剂是( )
A.C
B.C和S
C.KNO3
D.S和KNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统的生物脱氮工艺如下图所示,生物脱氮主要包括有氧条件下的硝化反应过程和缺氧环境下的反硝化反应过程。硝化过程中,NH4+先后氧化为NO2和NO2-。
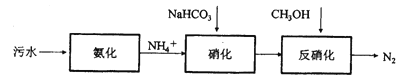
(1) NH4+在硝化过程中会使溶液酸度提高,需要加入NaHCO3进行中和。请写出NH4+硝化生成NO2-的离子方程式_________。
(2)①反硝化反应过程中,加入碳源(甲醇等有机物)将硝化反应中生成的NO2和NO2-还原为N2,如3CH3OH +6NO2-= 3N2↑+3CO2+3H2O+6OH-。新型生物脱氮工艺(SCND)可将硝化过程中的产物控制在NO2阶段,防止生成NO2-,该工艺的优点是_________。
②同步硝化反硝化工艺(SND)将硝化阶段和反硝化阶段放在同一个反应器中进行,该法既有SCND法的优点,将硝化过程中的产物控制在NO2-阶段,还有一个优点是___________。
③现在很多国家采用半硝化工艺(ANAMMOX),工作原理如下图所示:

半硝化脱氮反应器中,一半的NH4+氧化成NO2-,写出厌氧氨氧化发生反应的离子方程式_____。该方法是否需要加入碳源(甲醇),并简述原因________。
(3)研究发现,脱氮工艺会产生-一种温室气体N2O。目前普遍认为在硝化阶段会形成N2O,试分析N2O的成因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示渗透作用装置图,其中半透膜为膀胱膜,甲、丙装置中A、B、a、b溶液浓度分别用MA、MB、Ma、Mb表示,乙、丁装置分别表示一段时间后甲、丙装置的状态,液面上升的高度分别为h1、h2。如果A、B、a、b均为蔗糖溶液,且MA>MB,Ma=Mb>MA,则达到平衡后( )


A. h1>h2、Ma>MbB. h1>h2、Ma<Mb
C. h1<h2、Ma<MbD. h1<h2、Ma>Mb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 基态Si原子中,电子占据的最高能层符号为________,该能层具有的原子轨道数为_________。
(2) CH3COOH中C原子轨道杂化类型为_________;1molCH3COOH分子含有σ键的数目为_________。
(3) 复化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。

①基态硼原子的电子排布式为__________。
②六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为__________,分析其结构,与石墨相似却不导电,原因是__________。
③NH4BF4 (氟硼酸铵)是合成氮化硼纳米管原料之一。1mol NH4BF4 含有__________mol 配位键。
(4) Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______,微粒之间存在的作用力是__________。
(5) 晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为金刚石的晶胞,其中原子坐标参数A为(0,0 ,0);B为(![]() ,0,
,0, ![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为__________。
,0)。则D原子的坐标参数为__________。
②晶胞参数,描述晶胞的大小和形状,已知金刚石晶胞参数acm,其密度为__________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.0 g NaOH和5.3 g Na2CO3混合并配成溶液,向溶液中逐滴缓慢滴加0.5 mol/L稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的体积(标况下)的关系的是
A.  B.
B. 
C.  D.
D. 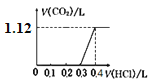
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件、医药及化工等领域。以辉锑矿为原料制备金属锑,其一种工艺流程如下:

己知部分信息如下:
I.辉锑矿(主要成分为Sb2S3,还含有As2S5、PbS 、CuO和SiO2等);
II.浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AsCl3和PbCl2等杂质;
III.常温下,Ksp(CuS)=1.0×10-36 Ksp(PbS)=9.0×10-29
回答下列问题:
(1)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是________(填化学式)。
(2)写出“还原”反应的化学方程式:______________ 。
(3)已知:浸出液中:c(Cu2+)=0.01 mol·L-1、c(Pb2+)=0.10 mol·L-1。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是_______(填化学式);当CuS、PbS共沉时,![]() =_________。加入硫化钠的量不宜过多,原因是_________。
=_________。加入硫化钠的量不宜过多,原因是_________。
(4)在“除砷”过程中,氧化产物为H3PO4。该反应中氧化剂、还原剂的物质的量之比___________。
(5)在“电解”过程中,以惰性材料为电极,阴极的电极反应式为______;“电解”中锑的产率与电压大小关系如图所示。当电压超过U0V时,锑的产率降低的原因可能是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组研究NaClO溶液与KI溶液的反应,实验记录如下:
实验编号 | 实验操作 | 实验现象 |
Ⅰ |
| ⅰ.溶液变为浅黄色 ⅱ.溶液变蓝 |
Ⅱ |
| ⅰ.溶液保持无色 ⅱ.溶液不变蓝,溶液的pH=10 |
【资料】:碘的化合物主要以I和IO3的形式存在。酸性条件下IO3不能氧化Cl,可以氧化I。ClO在pH<4并加热的条件下极不稳定。
(1)0.5 mol·L1 NaClO溶液的pH=11,用离子方程式表示其原因:______。
(2)实验Ⅰ中溶液变为浅黄色的离子方程式是______。
(3)对比实验Ⅰ和Ⅱ,研究实验Ⅱ反应后“溶液不变蓝”的原因。
① 提出假设a:I2在碱性溶液中不能存在。设计实验Ⅲ证实了假设a成立,实验Ⅲ的操作及现象是______。
② 进一步提出假设b:NaClO可将I2氧化为IO3。进行实验证实了假设b成立,装置如下图,其中甲溶液是______,实验现象是______。

(4)检验实验Ⅱ所得溶液中的IO3:
取实验Ⅱ所得溶液,滴加稀硫酸至过量,整个过程均未出现蓝色,一段时间后有黄绿色刺激性气味的气体产生,测得溶液的pH=2。再加入KI溶液,溶液变蓝,说明实验Ⅱ所得溶液中存在IO3。
① 产生的黄绿色气体是______。
② 有同学认为此实验不能说明实验Ⅱ所得溶液中存在IO3,理由是______。欲证明实验Ⅱ所得溶液中存在IO3,改进的实验方案是______。
③ 实验Ⅱ中反应的离子方程式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com