
【题目】A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常谧常压下有三种是气体,三种是固体。C和D两种元素按个数比l:l形成的化合物M,A和C两种元素按个数比2:1形成化合物N。
请回答下列问题:
(1)写出F在周期表中的位置_______,画出D的离子结构示意图_________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为________。
(3)C与F形成的常见化合物属于_______化合物(填“共价”或“离子”)。
(4)画出B单质的结构式_________。科学家合成出了B元素形成的B5n+电子式![]() ,则n值为__________。
,则n值为__________。
(5)化合物M属于_______化合物(填“共价”或“离子”),如何证明?___________。用电子式表示其形成过程______________。
(6)化合物M和化合物N反应的化学方程式:________________。
【答案】 第三周期第ⅥA族 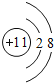
![]() 共价 N≡N l 离子 检验方法为验证其熔融态是否导电,若导电则为离子化合物,若不导电则为共价化合物。
共价 N≡N l 离子 检验方法为验证其熔融态是否导电,若导电则为离子化合物,若不导电则为共价化合物。 ![]() 2Na2O2+2H20=4NaOH+O2
2Na2O2+2H20=4NaOH+O2
【解析】A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,则A为氢元素;C元素的原子最外层电子数是次外层电子数的三倍,C原子有2个电子层,最外层电子数为6,故C为氧元素;C与F为同一主族,则F为硫元素;A与D为同一主族,且D的原子序数大于氧元素,D是所在周期原子半径最大的元素,故D为Na元素;六种元素所形成的常见单质在常温压下有三种是气体,三种是固体,故B、E的单质一种为气体、一种为固体,E的原子序数大于钠元素小于硫元素,故E为固体、B为气体,B的原子序数小于氧元素,则B为氮元素;由(3)可知,E是非金属元素,其单质在电子工业中有重要应用,则E为Si元素. C和D两种元素按个数比l:l形成的化合物M,M为Na2O2,A和C两种元素按个数比2:1形成化合物N,N为H2O。
(1)F为S元素,处于周期表中:第三周期ⅥA族,D的离子为Na+,离子结构示意图为: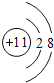 ,故答案为:第三周期ⅥA族;
,故答案为:第三周期ⅥA族;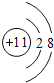 ;
;
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,则X为H2O2,Y为H2O,X的电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)C与F形成的常见化合物为二氧化硫、三氧化硫,均为共价化合物,故答案为:共价;
(4)B单质是氮气,结构式为N≡N;根据B5n+电子式![]() 可知 B5n+含有的电子数为8+8+8+2×5=34,核内的质子数为7×5=35,则n=35-34=1,故答案为:N≡N;l;
可知 B5n+含有的电子数为8+8+8+2×5=34,核内的质子数为7×5=35,则n=35-34=1,故答案为:N≡N;l;
(5)化合物M为过氧化钠,属于离子化合物,检验离子化合物的方法为验证其熔融态是否导电,若导电则为离子化合物,若不导电则为共价化合物。用电子式表示其形成过程为![]() ,故答案为:离子;检验方法为验证其熔融态是否导电,若导电则为离子化合物,若不导电则为共价化合物;
,故答案为:离子;检验方法为验证其熔融态是否导电,若导电则为离子化合物,若不导电则为共价化合物;![]() ;
;
(6)过氧化钠和水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2,故答案为:2Na2O2+2H2O=4NaOH+O2。


科目:高中化学 来源: 题型:
【题目】下列各组离子在指定条件下,一定大量共存的是
A. 在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+
B. pH=1的溶液中: Cu2+、Al3+、SO42-、NO3-
C. 能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-
D. 水电离出的c(H+)=1×10-12 mol/L的溶液中:Na+、Mg2+、Cl-、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】换位合成法在化学工业中每天都在应用,主要用于研制新型药物和合成先进的塑料材料。在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%。①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应 ⑥消去反应 ⑦加聚反应 ⑧缩聚反应等反应类型中能体现这一原子最经济原则的是 ( )
A.①②⑤ B.②⑤⑦ C.⑦⑧ D.只有⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从人类社会发展的长远前途看,对能源利用最好的办法是( )
A.大力勘探和开采石油
B.多利用天然气少使用石油
C.因为煤的储量比石油丰富,应多使用煤作能源
D.大力发展核能、氢能并充分利用太阳能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用量筒量取液体,量筒放平稳后仰视液面读得数值为19mL,倾倒部分液体后,又俯视液面,读得数值为10mL.则该学生实际倾倒的液体体积是
A. 9mL B. 小于9mL
C. 大于9mL D. 因操作错误无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中进行的可逆反应:aA(g)+bB(g)![]() cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是
cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种综合处理SO2废气的工艺流程。下列说法正确的是

A. 向B溶液中滴加KSCN溶液,溶液变为血红色
B. 溶液B转化为溶液C发生的变化的离子方程式为4H++2Fe2++O2=2Fe3++2H2O
C. 溶液酸性A>B>C
D. 加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液一定呈酸性的是
A.pH=6.8的溶液
B.常温下,由水电离的OH﹣离子浓度为1×10﹣13mol/L
C.加入酚酞,不显红色的溶液
D.常温下,溶液中的H+离子浓度为5×10﹣7mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com