
【题目】下列关于有机化合物的说法正确的是( )
A. 聚合物![]() 可由单体CH3CH=CH2和CH2=CH2加聚制得
可由单体CH3CH=CH2和CH2=CH2加聚制得
B. 戊烷(C5H12)有两种同分异构体
C. 乙烯、聚乙烯和苯分子均含有碳碳双键
D. 糖类、油脂和蛋白质均可发生水解反应
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)原电池中发生的化学反应属于________,原电池将________能转化成________能。
(2)如图为铜锌原电池:此电池中锌做________(填:正或负)极,发生________(填:氧化或还原)反应;铜极的电极方程式为________,电子流动的方向是:________(填:铜→锌或锌→铜)。
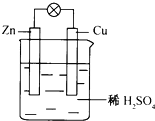
(3)工业上冶炼金属钠的方程式为:________,冶炼方法是:________;氧化铁和铝粉发生铝热反应的化学方程式为:________。铝热反应的用途:________(写出一种);工业上常用乙烯和水在一定条件下制取乙醇,其化学方程式为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1克氢气完全燃烧成水蒸气放出121kJ,1 mol O=O键完全断裂吸收496 kJ,1 mol H—O键形成时放出463 kJ,则氢气中1 mol H—H键断裂时吸收能量为( )
A.920 kJB.557 kJC.436 kJD.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为V L的密闭容器里进行反应,M、N的物质的量随时间的变化曲线如图所示,且两者都为气体:
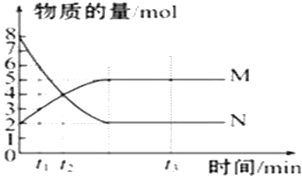
(1)此反应的化学方程式为__________________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:__________________。
(3)达平衡时N的转化率为:_______________ ;
(4)反应前与达平衡时容器内压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将下列物质分别装入有水的锥形瓶里(见下图),立即塞紧带 U 形管的塞子, 发现 U 形管内滴有红墨水的水面如图所示状态,判断加入的物质不可能是( )
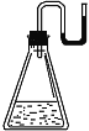
A.NaOH 固体B.浓硫酸C.![]() 晶体D.CaO固体
晶体D.CaO固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。

(1)Fe还原水体中NO3-的反应原理如图1所示。
①作负极的物质化学式为___________。
②正极的电极反应式是_________________________________________。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是_____________________________________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如图2所示,可得到的结论是____________________。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4,该反应的离子方程式为_________,解释加入Fe2+提高NO3-去除率的原因:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)=![]() v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有
mol,有![]() molD生成。回答下列问题:
molD生成。回答下列问题:
(1)反应2min内,v(A)=______________;v(B)=______________;
(2)下列叙述能说明该反应已达平衡状态的是:______;
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(3)反应平衡时,D为2amol,则B的转化率为________;
(4)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率_____(是“增大”“减小”或“不变”),
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com