
����Ŀ��ȼú�����Ṥҵβ���е�SO2����Ҫ�Ĵ�����Ⱦ����������·�������β���е�SO2��
����һ��ͨ������̿���û���
��1����ƽ��Ӧ����ʽ��____C(s)+____SO2(g)![]() _____S2(g)+_____CO2(g)
_____S2(g)+_____CO2(g)
��2����Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ______________________������ij�ܱ������н���������Ӧ��Ϊ�˼ӿ�����SO2���ɲ�ȡ�Ĵ�ʩ��_____________________________��
����������������������Һ��������
��3����β����������������ͨ�뵽��������������Һ�У��������������ƣ�pHֵ�ı仯��ͼ��ʾ�������ͼʾ������pHֵ�仯��ԭ��_________________________________________��

��������������������Ķ��������ڻ���̿���������·�Ӧ��ȡ�Ȼ�������SO2(g)+Cl2(g)![]() SO2Cl2(l)+97.3kJ����֪�Ȼ�������SO2Cl2����Ҫ�����Ȼ���������һ����ɫҺ�壬�۵�-54.1�棬�е�69.1�档
SO2Cl2(l)+97.3kJ����֪�Ȼ�������SO2Cl2����Ҫ�����Ȼ���������һ����ɫҺ�壬�۵�-54.1�棬�е�69.1�档
��4������Ӧ���������Ϊ2L��2������Һ������������2.7�ˣ���������ʾ���������ڵĻ�ѧ��Ӧ����____��
��5��������д��һ�ִ�ʩ���ɣ������ڴ������£�Ϊ�����SO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______________����___________________________ʱ˵��������Ӧ�Ѵﵽƽ��״̬��
���𰸡�2 2 1 2 K=![]() �����¶Ȼ�����ѹǿ��ʹ���ʵ������� ����������Һ����ˮ��ʼ���(pH>7)����ͨ�����������������������������ƣ���HSO3-���루��������ԣ��̶ȴ�����ˮ�⣨ˮ��ʼ��ԣ��̶ȣ�������Һ�����ԡ����Ŷ��������ͨ�룬��������Ũ����С������������Ũ��������һֱ����Ӧ��ȫ����pHֵ��Сֱ������ 0.005mol/(L��min) �����¶Ȼ�����ѹǿ ��������ɫ���ٸı��Һ���������ٸı�ȵ�
�����¶Ȼ�����ѹǿ��ʹ���ʵ������� ����������Һ����ˮ��ʼ���(pH>7)����ͨ�����������������������������ƣ���HSO3-���루��������ԣ��̶ȴ�����ˮ�⣨ˮ��ʼ��ԣ��̶ȣ�������Һ�����ԡ����Ŷ��������ͨ�룬��������Ũ����С������������Ũ��������һֱ����Ӧ��ȫ����pHֵ��Сֱ������ 0.005mol/(L��min) �����¶Ȼ�����ѹǿ ��������ɫ���ٸı��Һ���������ٸı�ȵ�
��������
��1��CԪ�صĻ��ϼ���0���ߵ�+4��SԪ�صĻ��ϼ���+4���͵�0�����ݻ��ϼ����ߺͽ��͵�������ȣ���ƽ�ĵĻ�ѧ����ʽΪ��2C(s)+ 2SO2(g)![]() S2(g)+ 2CO2(g)��
S2(g)+ 2CO2(g)��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=![]() ������ij�ܱ������н���������Ӧ��Ϊ�˼ӿ�����SO2������Ӱ�컯ѧ��Ӧ���ʵ������֪���ɲ�ȡ�Ĵ�ʩ�������¶ȡ�����ѹǿ��ʹ���ʵ������ȡ�
������ij�ܱ������н���������Ӧ��Ϊ�˼ӿ�����SO2������Ӱ�컯ѧ��Ӧ���ʵ������֪���ɲ�ȡ�Ĵ�ʩ�������¶ȡ�����ѹǿ��ʹ���ʵ������ȡ�
��3����β����������������ͨ�뵽��������������Һ�У��������������ơ�����pHֵ�ı仯ʾ��ͼ��֪����Һ�ɼ������ɵ����ԡ����ԣ����������ֲ��䡣pHֵ�������ֱ仯��ԭ���ǣ�����������Һ����ˮ��ʼ���(pH>7)����ͨ�����������������������������ƣ�HSO3-���루��������ԣ��̶ȴ�����ˮ�⣨ˮ��ʼ��ԣ��̶ȣ�������Һ�����ԡ����Ŷ��������ͨ�룬��������Ũ����С������������Ũ��������һֱ����Ӧ��ȫ�����õ�����������������Һ��������ı�����Һ����pHֵ��Сֱ�����䡣
��4������Ӧ���������Ϊ2L��2������Һ������������2.7�ˣ���2����������SO2Cl2(l)�����ʵ���Ϊ0.02mol������Ҫͬʱ����0.02mol������������ʾ���������ڵĻ�ѧ��Ӧ����Ϊ![]() 0.005mol/(L��min)��
0.005mol/(L��min)��
��5��SO2(g)+Cl2(g)![]() SO2Cl2(l)+97.3kJ���÷�ӦΪ������������ٵķ��ȷ�Ӧ�������¶Ȼ�����ѹǿ����ʹ�û�ѧƽ��������Ӧ�����ƶ������ڴ������£�Ϊ�����SO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�н����¶Ȼ�����ѹǿ����ƽ��״̬�£�����ֵ�Ũ�ȱ��ֲ��䣬����ֵ�����Ҳ���ֲ��䣬����ֻ����������ɫ�����壬�ʵ���������ɫ���ٸı��Һ���������ٸı�ʱ˵��������Ӧ�Ѵﵽƽ��״̬��
SO2Cl2(l)+97.3kJ���÷�ӦΪ������������ٵķ��ȷ�Ӧ�������¶Ȼ�����ѹǿ����ʹ�û�ѧƽ��������Ӧ�����ƶ������ڴ������£�Ϊ�����SO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�н����¶Ȼ�����ѹǿ����ƽ��״̬�£�����ֵ�Ũ�ȱ��ֲ��䣬����ֵ�����Ҳ���ֲ��䣬����ֻ����������ɫ�����壬�ʵ���������ɫ���ٸı��Һ���������ٸı�ʱ˵��������Ӧ�Ѵﵽƽ��״̬��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�صĻ������ڶ�������о�����ҪӦ�á�
��1��Mn2����̬��������Ų�ʽΪ________��SO42-��Sԭ�ӹ�����ӻ�����Ϊ________��
��2�������̵�3�����ӻ�������۵����±���
���� | MnCl2 | MnS | MnO |
�۵� | 650�� | 1610�� | 2800�� |
�ϱ�3�������о�����������________��
��3��ij��������ľ����ṹ��ͼ��ʾ����������Ļ�ѧʽΪ________��
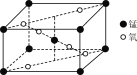
��4���ڻ�����K3[Mn(CN)6]�У���֮����ڵ���������________(����ĸ)��
a. ���Ӽ� b. ���ۼ� c. ��λ�� d. ���
��5���Ʊ�LiMn2O4��ʵ��������£���MnO2��Li2CO3��4��1�����ʵ���֮�����ϣ���ĥ3��5 h��Ȼ�����£����¼��ȣ�����24 h����ȴ�����¡�д���÷�Ӧ�Ļ�ѧ����ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C�������������ģ������ͼ��

��1��������������������ȫȼ��ʱ��ȥO2����������________(���Ӧ��ĸ����ͬ)��
��2��ͬ״����ͬ�������������������ȫȼ��ʱ��ȥO2����������____________��
��3����������������������ȼ��ʱ�����ɶ�����̼������________������ˮ������________��
��4����120����1.01��105 Pa��ʱ����������̬����������������ϵ�ȼ����ͬ�����²�÷�Ӧǰ���������û�з����仯��������������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ֱ�����ͼ��ʾװ�ö�ԭ��غ͵��ԭ������ʵ��̽����

��ش�
I����ͼ1��ʾװ�ý��е�һ��ʵ�顣
��1���ڱ�֤�缫��Ӧ���������£��������Cu���缫����_________������ĸ��ţ���
A���� | B��ʯī | C���� | D���� |
��2��N��������Ӧ�ĵ缫��ӦʽΪ____________________��
��3��ʵ������У�SO42-_________�����������������������������������������ƶ���
��ֽ���ܹ۲쵽��������___________________��
II����ͼ2��ʾװ�ý��еڶ���ʵ�顣ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���塣�������Ϸ��֣����������FeO42-������Һ�г��Ϻ�ɫ��
��4���������У�X������Һ��pH___________������������ ������С�����������������������У�Y�������ĵ缫��ӦΪFe-6e-+8OH-=FeO42-+4H2O ��_______________��
��5������X���ռ���672 mL���壬��Y���ռ���168 mL���壨��������Ϊ��״��ʱ�������������Y�缫�����缫����������________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��绯ѧ��ʴ��������װ������ͼ��ʾ�������й�˵����������� ��

A. dΪʯī����Ƭ��ʴ�ӿ�
B. dΪʯī��ʯī�ϵ缫��ӦΪ��O2 + 2H2O + 4e == 4OH�C
C. dΪп�飬��Ƭ���ױ���ʴ
D. dΪп�飬��Ƭ�ϵ缫��ӦΪ��2H+ + 2e == H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���ձ���ʢ�к�ˮ���������б���ʴ����ʴ�������ɿ쵽����˳��Ϊ

A. �ݢڢ٢ۢ� B. �ݢܢڢ٢�
C. �ܢۢڢ٢� D. �ۢڢܢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ��������еĻ�ѧ��Ӧ��Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)�����������в���ȷ����(����)

A. Zn��H2SO4������������ZnSO4��H2��������
B. ��Ӧ������������ϵ������ͼ��ʾ
C. �����÷�Ӧ��Ƴ�ԭ��أ���ZnΪ����
D. �����÷�Ӧ��Ƴ�ԭ��أ�����32.5gп�ܽ�ʱ�����ų�22.4 L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��NO��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣���÷�Ӧ6NO2��g��+8NH3��g��![]() 7N2��g��+12H2O��g���ɴ���NO2��
7N2��g��+12H2O��g���ɴ���NO2��
��1����2L���ܱ������У�2�����ڣ�������Ӧ���������ʵ���������0.25mol����2������v��NH3��=______��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=______����֪�÷�Ӧƽ�ⳣ����K�����¶ȣ�T���Ĺ�ϵ��ͼ��ʾ���������¶ȣ���v����Ӧ______v�淴Ӧ������ڡ�����С�ڡ����ڡ�������Ӧ�ﵽƽ�������С��Ӧ��������������������䣬���������ƽ��ʽ����______����������С�����䡱����
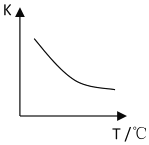
�����Ǵ�����Ⱦ��Σ��֮һ����������SO2���ĺ����ǿ�����������һ����Ҫָ�ꡣij��ȤС��ͬѧ�ռ�ij�ص���ˮ����ʵ�飬ÿ��1h��ͨ��pH�Ʋⶨ��ˮ��Ʒ��pH����õĽ�����±���
�ⶨʱ��/h | 0 | 1 | 2 | 3 | 4 |
��ˮ��Ʒ��pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
��3����д������pH�仯��ԭ��______��
��4�������ʵ���Ũ����ȵ����������Һ����NH4Cl ��NH4HCO3 ��NH4HSO4����������Һ��ˮ�ĵ���̶��ɴ�С��˳����______�����ţ���
��5����BaCl2��Һ��ͨ������SO2���壬û�г������ɣ������μ�һ�����İ�ˮ������BaSO3�������õ���ƽ��ԭ��������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1 g������ȫȼ������ˮ����ʱ�ų�����121 kJ����������1 mol O=O����ȫ����ʱ��������496 kJ��ˮ������1mol H-O���γ�ʱ�ų�����463 kJ����������1mol H-H������ʱ��������Ϊ
A.920 kJB.557 kJC.436 kJD.188 kJ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com