
已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的成分,主要操作流程如下图:
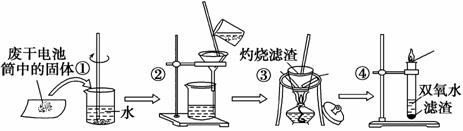
试回答下列问题。
(1)步骤①用玻璃棒搅拌的目的是_______________________________________
___________________________________________________________________;
步骤②过滤后,滤液中的主要溶质有____________(填化学式);步骤③中灼烧的目的是__________________________________ ______________________________________。
______________________________________。
(2)经过步骤③得到的是粗制二氧化锰,要得到精制的二氧化锰还需将粗制二氧化锰用稀硝酸洗涤和蒸馏水洗涤,稀硝酸的作用是___________________________________
______ ______________________________________________________________。
______________________________________________________________。
(3)写出步骤④中发生反应的化学方程式:__________________________________
________________________________________________________________________,
经过步骤②得到的固体干燥后,用氯酸钾与之混合加热的实验________(填“能”或“不能”)代替实验④。
(4)已知NH4Cl和ZnCl2的溶解度(g/100 g水)如下表:
| 温度(℃) | 20 | 30 | 40 | 60 | 80 |
| NH4Cl | 37.2 | 31.4 | 45.8 | 65.6 | 77.3 |
| ZnCl2 | 396 | 437 | 452 | 541 | 614 |
从滤液中分离NH4Cl和ZnCl2的方法是___________________________________。
(5)从有害物质必须特殊处理的角度考虑,上述设计不合理的地方是___________________________________ _____________________________________。
_____________________________________。
解析 (1)溶解时用玻璃棒搅拌的主要目的是加速其中的电解质溶解于水;废干电池中的氯化铵和氯化锌可溶于水;灼烧的目的是除去滤渣中的炭黑和淀粉等有机物。(2)Mn2O3及其中的其他金属氧化物能溶于稀硝酸,MnO2不溶于稀HNO3从而分离。(3)二氧化锰能催化过氧化氢分解放出氧气,从而间接检验二氧化锰,直接用含有机物的不纯二氧化锰与氯酸钾作用会引起爆炸。(4)由溶解度数据知,两者溶解度相差很大,先蒸发溶剂然后冷却结晶就可得较纯净的氯化铵晶体。
答案 (1)促进废干电池筒中的可溶性物质溶解 ZnCl2、NH4Cl 除去其中的炭黑和有机物 (2)除去其中的低价锰的氧化物和其他金属化合物 (3)2H2O2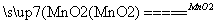 2H2O+O2↑ 不能 (4)结晶(重结晶) (5)没有回收有害物质汞,在实验过程中会产生汞蒸气污染
2H2O+O2↑ 不能 (4)结晶(重结晶) (5)没有回收有害物质汞,在实验过程中会产生汞蒸气污染


科目:高中化学 来源: 题型:
下列离子方程式错误的是
A.硅酸钠溶液中通入CO2气体 SiO32- + H2O + CO2 = H2SiO3↓+ CO32-
B.硫酸铝与过量氨水反应 Al3+ + 4NH3·H2O = AlO2-↓+ 4NH4+ + 2H2O
C.氯气与氢氧化钠溶液反应Cl2+2OH- = Cl- + ClO- + H2O
D.碳酸氢钠溶液与稀盐酸反应 HCO3- + H+ = H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分离方法正确的是
A.分离汽油和水可以用结晶的方法
B.除去氯化钠溶液中的泥沙用分液的方法
C.分离乙酸(沸点118 ℃)与乙酸乙酯(沸点77.1 ℃)用蒸馏的方法
D.从含有少量氯化钠的硝酸钾溶液中提取硝酸钾用过滤的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,所选装置不合理的是
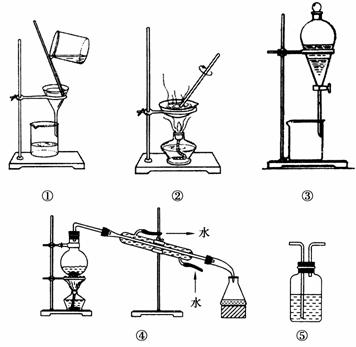
A.分离Na2CO3溶液和CH3COOC2H5,选④
B.用CCl4提取碘水中的碘,选③
C.用FeCl2溶液吸收Cl2,选⑤
D.粗盐提纯,选①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
为检验下列物质是否已被氧化,所选试剂(括号内物质)不正确的是( )
A.氯化亚铁溶液(硫氰化钾溶液)
B.碘化钾溶液(淀粉溶液)
C.乙醛(紫色石蕊试液)
D.亚硫酸钠溶液(氯化钡溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是( )
A.将铜屑加入Fe3+溶液中:2Fe3++Cu===2Fe2++Cu2+
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+===3Fe3++4H2O
C.将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO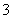 ===3Fe3++2H2O+NO↑
===3Fe3++2H2O+NO↑
D.将铁粉加入稀硫酸中:2Fe+6H+===2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
[提出假设]
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO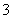 能氧化Ag。
能氧化Ag。
[设计实验方案,验证假设]
(1)甲同学从上述实验的生成物中检验出Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:
________________________________________________________________________。
(2)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO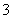 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立若银镜不消失,假设2不成立 |
[思考与交流]
(3)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO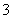 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论,并简述理由:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
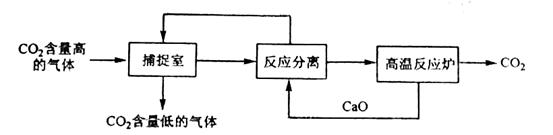
下列有关该方法的叙述中正确的是
A.能耗大是该方法的一大缺点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com