
【题目】下图所表示的一些物质或概念间的从属关系不正确的是

X | Y | Z | |
A | 置换反应 | 氧化还原反应 | 离子反应 |
B | 冰水混合物 | 电解质 | 化合物 |
C | 淀粉溶液 | 胶体 | 分散系 |
D | 干冰 | 氧化物 | 纯净物 |
A. AB. BC. CD. D
科目:高中化学 来源: 题型:
【题目】乙二胺(H2NCH2CH2NH2 )是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是
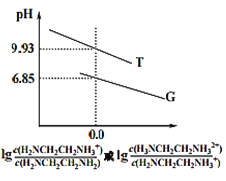
A. Kb2[H2NCH2CH2NH2] 的数量级为10-8
B. 曲线G代表pH 与![]() 的变化关系
的变化关系
C. H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-)
D. 0.01mol·L-1H2NCH2CH2NH2 电离度约为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为______。
(2)下列关于CH4和CO2的说法正确的是______(填序号)。
a.固态CO2属于分子晶体
b. CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为____________,Ni该元素位于元素周期表的第___族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有_____molσ键。
(4)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”。
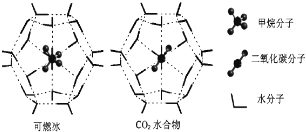
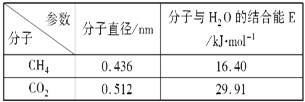
①“可燃冰”中分子间存在的2种作用力是______。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。基态Ni原子的外围电子排布式为 ,该元素位于元素周期表中的第 族。
(2)碳元素能够形成不同的单质,如C60、C70、金刚石等等。
①C60、C70、金刚石这些单质间互称为 。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。

③继C60后,科学家又合成了Si60、N60, C、Si、N三种原子电负性由大到小的顺序是 。
(3)铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
①Cu位于元素周期表第ⅠB族。Cu2+的核外电子排布式为 。
②Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,粗盐精制的实验流程如下。下列说法不正确的是
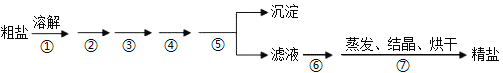
A. 在第①步中使用玻璃棒搅拌可加速粗盐溶解
B. 第⑤步操作是过滤
C. 在第②③④⑥步通过加入化学试剂除杂,加入试剂顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→稀盐酸
D. 除去MgCl2的离子方程式为:Mg2++2OH=Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molCO和2molH2充入密闭容器中,发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H。在其他条件相同时,测得CO平衡转化率[α(CO)]与温度和压强的关系如下图。
CH3OH(g) △H。在其他条件相同时,测得CO平衡转化率[α(CO)]与温度和压强的关系如下图。
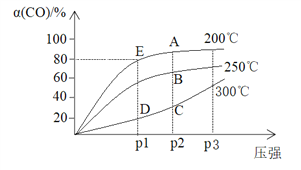
下列说法不正确的是
A. △H <0
B. C、D两点的反应速率:v(C)> v(D)
C. 若E点的容器体积为10L,该温度下的平衡常数为k=25
D. 工业生产中实际控制的条件200℃、P2压强,不采用P3的理由是,增大压强转化率变化不大,而且工业成本调高,得不偿失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项正确的是( )
A. 镁、铝与沸水不可能反应
B. 铁在一定条件下可以与水反应
C. 钠与水反应的离子方程式:Na+H2O=Na++OH-+H2↑
D. 钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+=2Na++Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中没有沉淀出现的是
A. 向常温时的饱和碳酸钠溶液中通入足量CO2气体 B. 向硅酸钠溶液中通入氯化氢气体
C. 向氯化钙溶液中通入SO2气体 D. 向次氯酸钙溶液中通入CO2气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com