
【题目】(1)将12.7g 固态碘与氢气完全反应生成碘化氢气体时,吸收2.604kJ的热量,该反应的热化学方程式为____________________。
(2)用 NA表示阿伏加德罗常数,在 C2H2(气态)完全燃烧生成 CO2和液态水的反应中,每有5NA个电子转移时,放出 650kJ 的热量。则表示 C2H2(气态) 燃烧热的热化学方程式为____________。
(3)发射卫星时,常用肼为燃料,NO2气体作氧化剂。
已知: N2(g)+2O2(g)=2NO2 (g) △H=+68kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ·mol-1
写出气态肼和NO2反应生成氮气和水蒸气的热化学方程式___________。
【答案】(1)I2(s)+H2(g)=2HI(g) △H=+52.08kJ·mol-1
(2)C2H2(g)+![]() O2(g)==2CO2(g)+H2O(l) △H=–1300kJ·mol-1
O2(g)==2CO2(g)+H2O(l) △H=–1300kJ·mol-1
(3)2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH=-1136kJ·mol-1
【解析】
试题分析:(1)12.7g 固态碘是0.05mol,与氢气完全反应生成碘化氢气体时,吸收2.604kJ的热量,则qmol碘完全反应吸收的热量是![]() =52.08kJ,因此该反应的热化学方程式为I2(s)+H2(g)=2HI(g)△H= +52.08kJ·mol-1。
=52.08kJ,因此该反应的热化学方程式为I2(s)+H2(g)=2HI(g)△H= +52.08kJ·mol-1。
(2)1mol乙炔完全燃烧失去电子的物质的量是[4-(-1)]×2=10mol,每有5NA个电子转移时,放出 650kJ 的热量。则1mol乙炔完全燃烧放出的热量是650kJ×2=1300kJ,因此表示 C2H2(气态) 燃烧热的热化学方程式为C2H2(g)+![]() O2(g) == 2CO2(g)+H2O(l) △H=–1300kJ·mol-1;
O2(g) == 2CO2(g)+H2O(l) △H=–1300kJ·mol-1;
(3)已知:① N2(g)+2O2(g)=2NO2 (g) △H=+68kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ·mol-1
则根据盖斯定律可知②×2-①即得到气态肼和NO2反应生成氮气和水蒸气的热化学方程式2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH=-1136kJ·mol-1。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】【2016湾里区模拟】在25℃、1.01×105 Pa下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJmol﹣1能自发进行的合理解释是( )
A.该反应是分解反应
B.该反应的熵增效应大于焓变效应
C.该反应是熵减反应
D.该反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
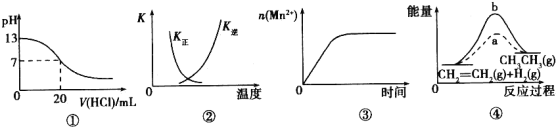
A.图①表示25℃时,用0.1 moI·L-1盐酸滴定20 mL0.l mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0, 正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH<0, 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.0l moI·L-1 KMnO4酸性溶液与过量的0.l moI·L-1H2C2O4 溶液混合时,n(Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)![]() CH3CH3(g) △H<0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g) △H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届北京市昌平区高三上学期期末】下列说法不正确的是
N2(g)与H2(g)在铁催化剂表面经历如下过程生成NH3(g):

A.Ⅰ过程中破坏的均为非极性键
B.Ⅰ过程吸收能量,II过程放出能量
C. N2(g) + 3H2(g) ![]() 2NH3(g) ΔH = –44 kJ·mol-1
2NH3(g) ΔH = –44 kJ·mol-1
D.1mol N2(g)与3 mol H2(g)所具有的总能量比2 mol NH3(g) 所具有的总能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
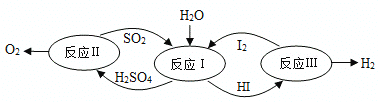
(1)反应Ⅰ的化学方程式是_______________________。
反应Ⅲ的化学方程式是____________________。
(2)SO2的排放是形成酸雨的原因之一,我们把pH小于_____的雨称为酸雨。
(3)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层,分别是含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是____________(选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②分离两层液体用到的玻璃仪器主要有_____________________。
③辨别两层溶液的方法是____________。
④经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是__________________________。
(4)反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g),已知生成9 g水蒸气吸收137.5 KJ的热量,写出该反应的热化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法中不正确的是

A.T℃时,在Y点和Z点,Ag2CrO4的Ksp相等
B.向饱和Ag2CrO4溶液中加入固体K2CrO4,能使溶液由Y点变到Z点
C.T℃时,Ag2CrO4的Ksp数值为1×10-8
D.图中a=![]() ×10-4
×10-4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017枣阳市校级一模】下列保存物质的方法正确的是( )
A.保存液溴时向其中加入少量酒精,减少挥发
B.氢氟酸保存在塑料塞的玻璃瓶中,防止瓶口和塞子粘住
C.氨水易挥发,应密封在低温处保存
D.金属锂应保存在煤油中,防止被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解,100℃左右时升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不相同,分别如(I)和(Ⅱ)所示,

试回答:
(1)B中反应的化学方程式为___________________________。
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是______________。
(3)D中反应的化学方程式为______________________________。
(4)装置(I)的主要缺点是_______________________。
(5)装置(Ⅱ)的主要缺点是______________________________,如果选用此装置来完成实验,则必须采取的改进措施是:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,二氧化碳(CO2)的排放量也要大幅减少。
(1)在恒温,容积为1 L恒容中,硫可以发生如下转化,其反应过程和能量关系如图1所示(已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
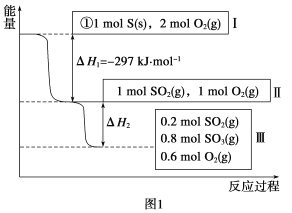
①写出能表示硫的燃烧热的热化学方程式:________。
②ΔH2=__________kJ·mol-1。
③在相同条件下,充入1 mol SO3和0.5 mol的O2,则达到平衡时SO3的转化率为___________;此时该反应________(填“放出”或“吸收”)________kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
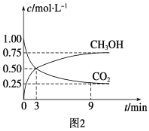
①CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
②能说明上述反应达到平衡状态的是________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
③为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有________(填编号)。
A.升高温度 B.缩小容器体积 C.再充入CO2气体 D.使用合适的催化剂
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应ΔS<0
C.在T ℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 MPa)和250 ℃,是因为此条件下,原料气转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com