
����Ŀ�����Ŵ�����Ⱦ���������أ�����������ʮ�������ڼ䣬����������(SO2)�ŷ�������8%����������(NOx)�ŷ�������10%��������̼(CO2)���ŷ���ҲҪ������١�
(1)�ں��£��ݻ�Ϊ1 L�����У�����Է�������ת�����䷴Ӧ���̺�������ϵ��ͼ1��ʾ(��֪:2SO2(g)��O2(g) ![]() 2SO3(g) ��H����196.6 kJ��mol��1)����ش���������:
2SO3(g) ��H����196.6 kJ��mol��1)����ش���������:
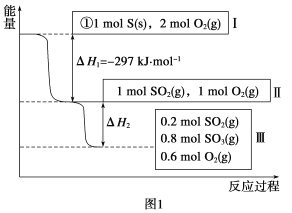
��д���ܱ�ʾ���ȼ���ȵ��Ȼ�ѧ����ʽ:________��
����H2��__________kJ��mol��1��
������ͬ�����£�����1 mol SO3��0.5 mol��O2����ﵽƽ��ʱSO3��ת����Ϊ___________����ʱ�÷�Ӧ________(�����ų�������������)________kJ��������
(2)�й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��
��CO2��ת�����л���ʵ��̼ѭ���������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�Ӧ:CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g) ��H����49.0 kJ��mol��1�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ2��ʾ����3 min��9 min��v(H2)��________mol��L��1��min��1��
CH3OH(g)��H2O(g) ��H����49.0 kJ��mol��1�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ2��ʾ����3 min��9 min��v(H2)��________mol��L��1��min��1��
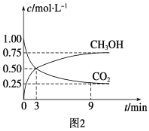
����˵��������Ӧ�ﵽƽ��״̬����________(����)��
A.��Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1��1(��ͼ�н����)
B.���������ܶȲ���ʱ��ı仯���仯
C.��λʱ��������3 mol H2��ͬʱ����1 mol H2O
D.CO2����������ڻ�������б��ֲ���
��Ϊ�˼ӿ컯ѧ��Ӧ������ʹ��ϵ����������ʵ������٣�������������ʱ���ɲ�ȡ�Ĵ�ʩ��________(����)��
A.�����¶� B.��С������� C.�ٳ���CO2���� D.ʹ�ú��ʵĴ���
(3)��ҵ�ϣ�CH3OHҲ����CO��H2�ϳɡ��ο��ϳɷ�ӦCO(g)��2H2(g) ![]() CH3OH(g)��ƽ�ⳣ��������˵����ȷ����________��
CH3OH(g)��ƽ�ⳣ��������˵����ȷ����________��
�¶�/�� | 0 | 100 | 200 | 300 | 400 |
ƽ�ⳣ�� | 667 | 13 | 1.9��10��2 | 2.4��10��4 | 1��10��5 |
A.�÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ
B.�÷�Ӧ�ڵ����²����Է����У������¿��Է����У�˵���÷�Ӧ��S<0
C.��T ��ʱ��1 L�ܱ������У�Ͷ��0.1 mol CO��0.2 mol H2���ﵽƽ��ʱ��COת����Ϊ50%�����ʱ��ƽ�ⳣ��Ϊ100
D.��ҵ�ϲ����Ըߵ�ѹǿ(5 MPa)��250 ��������Ϊ�������£�ԭ����ת�������
���𰸡�
(1)��S(s)��O2(g) = SO2(g) ��H����297 kJ��mol��1 ��
����78.64����20%�����գ�19.66 ��
(2)��0.125����D����B��
(3)AC��
��������
���������(1)��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ų������������ԣ�������ʵ���Ϊ1mol����ͼ1��֪1molS(s)��ȫȼ�շų�������Ϊ297KJ�����ԣ����ȼ���ȵ��Ȼ�ѧ����ʽS(s)+O2(g)�TSO2(g)��H=-297 KJmol-1���ʴ�Ϊ��S(s)+O2(g)�TSO2(g)��H=-297 KJmol-1��
������ͼ1��֪���μӷ�Ӧ��n(SO2)=1mol-0.2mol=0.8mol�������Ȼ�ѧ����ʽ��2SO2(g)+O2(g)2SO3(g)��H=-196.6KJmol- 1����֪����H2=0.4��H=0.4��(=-196.6KJmol- 1)=-78.64KJmol-1���ʴ�Ϊ��-78.64KJmol-1��
������ͬ�����£�����1 mol SO3��0.5 mol��O2���൱�ڳ���1 mol SO2��1molO2������ͼ����1 mol SO2��1molO2��ƽ��ʱSO2��ת����Ϊ![]() ��100%=80%����ﵽƽ��ʱSO3��ת����Ϊ20%���ֽ��SO3Ϊ0.2mol����ʱ�÷�Ӧ���յ�����Ϊ196.6��
��100%=80%����ﵽƽ��ʱSO3��ת����Ϊ20%���ֽ��SO3Ϊ0.2mol����ʱ�÷�Ӧ���յ�����Ϊ196.6��![]() =19.66 KJ���ʴ�Ϊ��20%�����գ�19.66 ��
=19.66 KJ���ʴ�Ϊ��20%�����գ�19.66 ��
(2)��v(CO2)=![]() =
=![]() =0.417mol/Lmin����v(H2)=3v(CO2)=3��0.417mol/Lmin=0.125mol/(Lmin)-1���ʴ�Ϊ��0.125��
=0.417mol/Lmin����v(H2)=3v(CO2)=3��0.417mol/Lmin=0.125mol/(Lmin)-1���ʴ�Ϊ��0.125��
��A����Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1��1ʱ��û�дﵽƽ��״̬����A����B��������������������䣬������������䣬�������Ƿ�ﵽƽ��״̬��������ܶȶ����䣬��B����C����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ������Ƿ�ﵽƽ��״̬�������ڵ�λʱ����ÿ����3molH2��ͬʱ����1molH2O����C����D��CO2����������ڻ�������б��ֲ��䣬˵���ﵽƽ��״̬����D��ȷ����ѡD��
��A.�����¶ȣ���Ӧ���ʼӿ죬ƽ�������ƶ�����������ʵ���������B.��С�����������Ӧ���ʼӿ죬ƽ�������ƶ�����������ʵ�����С����ȷ��C.�ٳ���CO2���壬��Ӧ���ʼӿ죬ƽ�������ƶ�����������ʵ���������D.ʹ�ú��ʵĴ�������Ӧ���ʼӿ죬ƽ�ⲻ�ƶ�����������ʵ������䣬����ѡB��
(3)A������ƽ�ⳣ�����¶ȱ仯��ƽ���ƶ�ԭ�������жϣ����¶�����ƽ�ⳣ����С������ӦΪ���ȷ�Ӧ��H��0����A��ȷ��B���÷�Ӧ���ڷ��ȷ�Ӧ����H��0���ڵ����²����Է����У������¿��Է����У�������G=��H-T��S��0��˵���÷�Ӧ��S��0����B����C�����ƽ������ʽ��ʽ���㣬ƽ�ⳣ������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻���
CO(g)+2H2(g)CH3OH(g)
��ʼ��(mol/L) 0.1 0.2 0
�仯��(mol/L) 0.1��50% 0.1 0.05
ƽ����(mol/L) 0.05 0.1 0.05
ƽ�ⳣ��K=![]() =100����C��ȷ��D������ƽ��������У��������Ǵ������������ԭ������ת���ʸߣ���D����ѡAC��
=100����C��ȷ��D������ƽ��������У��������Ǵ������������ԭ������ת���ʸߣ���D����ѡAC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����12.7g ��̬����������ȫ��Ӧ���ɵ⻯������ʱ������2.604kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ____________________��
��2���� NA��ʾ�����ӵ��������� C2H2����̬����ȫȼ������ CO2��Һ̬ˮ�ķ�Ӧ�У�ÿ��5NA������ת��ʱ���ų� 650kJ �����������ʾ C2H2����̬�� ȼ���ȵ��Ȼ�ѧ����ʽΪ____________��
��3����������ʱ��������Ϊȼ�ϣ�NO2��������������
��֪�� N2(g)��2O2(g)=2NO2 (g) ��H����68kJ��mol��1
N2H4(g)��O2(g)=N2(g)��2H2O(g) ��H����534kJ��mol��1
д����̬�º�NO2��Ӧ���ɵ�����ˮ�������Ȼ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е�������X��Y���ֽ������ֱ������������������ͬ������ϡ�����У����������������뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ����֪X��Y���������л��ϼ۾�Ϊ+2�ۣ���������˵���в���ȷ����

A. ����������������X��Y B. ���ԭ��������X��Y
C. ������ԣ�Y��X D. ���������������X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����DNA�ijɷ���
A. �������ǡ����������
B. �������ǡ����������
C. ���ǡ����������
D. ���ǡ����ʡ���ऺ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ������NH![]() ��Ũ����Cl����Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м���
��Ũ����Cl����Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м���
������������ ��������NaCl �������İ�ˮ��������NaOH
A���٢� B���� C���ۢ� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. �Ȼ������ˮ��ϵ�¶Ƚ��ͣ�����仯�����ȷ�Ӧ
B. ���������ȼ�ϣ�˵������ȼ���Ƿ��ȷ�Ӧ
C. ������������һ�����ڷ�Ӧ��������
D. ͬ��ͬѹ�£�H2��Cl2�ڹ��պ͵�ȼ�����µ���H��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֱ�Ӱ����飨NH3��BH3����ؿ��ڳ����¹�����װ����ͼ���õ�ص��ܷ�ӦΪ��NH3��BH3+3H2O=NH4BO2+4H2O������˵����ȷ���ǣ� ��

A. ���缫������ԭ��Ӧ
B. ��ع���ʱ��H��ͨ�����ӽ���Ĥ���ƶ�
C. �����ĵ缫��ӦʽΪ2H��+2e��=H2��
D. ����3.1g�����飬������ת��0.6mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���2L�����ܱ������г���1mol PCl5��������Ӧ��PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
��Ӧ�����вⶨ�IJ������ݼ��±�����Ӧ�������������䣩:
t/s | 0 | 50 | 150 | 250 | 350 | 450 | |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x | |
��ش���������:
(1) x ��ֵ��________��
(2) 0-50s �ڣ���PCl3��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������________��
(3)250s �Ժ�Cl2�����ʵ������ٸı��ԭ����_______________��
(4) 250s ʱ��������Cl2�����ʵ�����_____��PCl5�����ʵ�����______��PCl5��ת������______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com