
科目:高中化学 来源: 题型:
| A、甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 |
| B、苯与硝酸发生反应生成硝基苯,甲苯与硝酸反应生成三硝基甲苯 |
| C、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| D、苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲醚与乙醇是同分异构体 |
| B、甲醚可由甲醇在一定条件下发生消去反应而制得 |
| C、甲醚作燃料不会产生氮的氧化物和碳氢化合物的污染 |
| D、1mol甲醚完全燃烧消耗的氧气与1mol甲醇完全燃烧消耗的氧气相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铁在涂料工业中用作红色防锈颜料 |
| B、铝制餐具不宜用来长时间存放酸性、碱性食物 |
| C、硅胶可用作袋装食品、瓶装药品等的干燥剂 |
| D、二氧化硫具有漂白性,可以用于食品增白 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.15mol/L |
| D、0.25mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质子数、中子数均为1的核素:1H |
| B、漂白粉的有效成分的化学式:CaClO |
C、Cl-的离子结构示意图: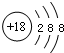 |
| D、碳酸钠的电离方程式:Na2CO3=2Na++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com