
下列实验方案中,不能测定Na2CO3和NaHCO3,混合物中Na2CO3质量分数的是
A.取a克混合物充分加热,建中b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。

【解析】NaHCO3受热易分解生成碳酸钠、水和二氧化碳,所以通过加热分解利用差量法即可计算出Na2CO3质量分数,A正确;Na2CO3和NaHCO3均可与盐酸反应生成水、二氧化碳和氯化钠,所以bg固体是氯化钠,利用守恒法可计算出Na2CO3质量分数,B正确;混合物与足量稀硫酸充分反应,也会生成水和二氧化,所以逸出的气体是二氧化碳,但会混有水蒸气,即碱石灰增加的质量不是 二氧化碳的质量,因此选项C不能测出混合物中Na2CO3质量分数;Na2CO3和NaHCO3都与Ba(OH)2反应,反应的方程式为
二氧化碳的质量,因此选项C不能测出混合物中Na2CO3质量分数;Na2CO3和NaHCO3都与Ba(OH)2反应,反应的方程式为
CO32-+Ba2+=BaCO3↓、HCO3-+OH-+Ba2+=H2O+BaCO3↓,因此最后得到的固体是BaCO3,所以可以计算出Na2CO3质量分数,选项D也正确。
【答案】C



科目:高中化学 来源: 题型:
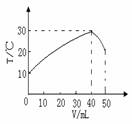
向盛有50mL 1.00 mol·L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如右图所示,下列不正确的是( )
A.该实验表明化学能可以转化为热能
B.NaOH溶液的浓度大于1.00 mol·L-1
C.V=50mL时,混合液的pH>7
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,
溶液的颜色变化情况是 ( )
A. 先变红色后变紫色 B. 变红后颜色不再改变
C. 先变无色后变红 D. 先变蓝色后变紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
从H、O、C、Ca四种元素中,选择适当的元素组成符合下列要求的一种物质,并
用化学式填空。
(1)具有可燃性,可做火箭燃料的是 。
(2) 相对分子质量最小的氧化物是 。
相对分子质量最小的氧化物是 。
(3)大理石或石灰石的主要成分都是  。
。
(4)可做温室肥料,固体可用于人工降雨的是 。
(5)农业上可供用来改良酸性土壤的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌

查看答案和解析>>
科目:高中化学 来源: 题型:
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。

已知:
① 反应 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
② I是一种常见的温室气体,它和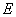 可以发生反应:2E+I
可以发生反应:2E+I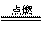 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为____________________________________________;
(2)化合物Ⅰ的电子式为______________________,它的空间构型是_________;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方 程式和计算过程);
程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________________,反应后溶液与过量化合物Ⅰ反应的离子方程式为_______________________________;
(5)E在I中燃烧观察到的现象是__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属及其合金的说法不正确的是( )
A.目前我国流通的硬币是由合金材料制造的
B.生铁、普通钢和不锈钢中的碳含量依次增加
C.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com