
| A. | 可逆反应的特征是正反应速率和逆反应速率相等 | |
| B. | 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 | |
| C. | 在其他条件不变时,升高温度可以使平衡向正反应方向移动 | |
| D. | 对于反应A(g)+3B(g)?2C(g)△H<0达平衡后,温度降低,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
分析 A.可逆反应为在相同条件下正反应和逆反应同时进行的反应,化学平衡状态的本质特征为同种物质的生成速率与消耗速率相等;
B.使用催化剂可以改变化学反应速率,但不能改变化学平衡状态;
C.升高温度可以使化学平衡向吸热反应的方向移动;
D.降低温度,正、逆反应速率都减小.
解答 解:A.可逆反应为在相同条件下正反应和逆反应同时进行的反应,正、逆反应速率相等为化学平衡状态的特征,不是可逆反应的特征,故A错误;
B.使用催化剂可以改变化学反应速率,但不能改变化学平衡状态,故B正确;
C.升高温度可以使化学平衡向吸热反应的方向移动,由于反应是吸热还是放热未知,不能确定平衡移动方向,故C错误;
D.降低温度,正、逆反应速率都减小,正反应为放热反应,平衡正向移动,正反应速率降低更少,故D错误,
故选:B.
点评 本题考查可逆反应、化学平衡状态特征、化学平衡影响因素、反应速率影响因素,理解掌握改变条件反应速率变化与平衡移动关系.


科目:高中化学 来源: 题型:选择题
| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 二氧化碳的水溶液能够导电,故二氧化碳属于电解质 | |
| C. | 碳酸氢钠在水中电离的离子方程式为NaHCO3═Na++H++CO32- | |
| D. | 碳酸钠属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素A的一种单质是太阳能电池中的主要材料 | |
| B. | 元素C的某单质与过氧化钠的漂白原理类似 | |
| C. | B和E可组成一种耐高温的结构材料,其化学式为E4B3 | |
| D. | 工业上制取E单质时,生成的气体主要是AO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
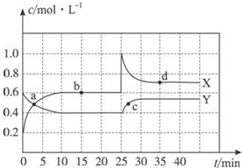 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水制取氢气 | |
| B. | 大量设立水电站,用电力分解水制取氢气. | |
| C. | 设法将太阳能聚焦,产生高温,使水分解产生氢气. | |
| D. | 寻找更多的化石燃料,利用其燃烧放热,使水分解产生氢气. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的戊烷含有分子数为0.5NA | |
| B. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA | |
| C. | 1mol甘氨酸(α-氨基乙酸)分子中存在9NA对共用电子 | |
| D. | 1L0.1mol/L的苯酚分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,硅甲烷的密度小于甲烷 | |
| B. | 硅甲烷燃烧生成二氧化硅和水 | |
| C. | 硅烷的分子通式可表示为SinH2n+2 | |
| D. | 硅甲烷与硅乙烷的相对分子质量相差30 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com