
| 选项 | 物质(括号内为杂质) | 除杂试剂 |
| A | CO(CO2) | 通入过量澄清石灰水 |
| B | CaCl2溶液(HCl) | 加适量Ba(OH)2溶液 |
| C | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| D | NaOH溶液(Na2CO3) | 加适量Ca(OH)2或Ba(OH)2溶液、过滤 |
分析 A.二氧化碳和与澄清石灰水反应;
B.生成氯化钡,引入新杂质;
C.生成盐酸,引入新杂质;
D.生成碳酸钡或碳酸钙沉淀,同时生成氢氧化钠.
解答 解:A.CO与澄清石灰水不反应,而二氧化碳和与澄清石灰水反应,可用于除杂,故A正确;
B.生成氯化钡,引入新杂质,应加入适量氢氧化钙除杂,故B错误;
C.生成盐酸,引入新杂质,应加入硝酸钡除杂,故C错误;
D.生成碳酸钡或碳酸钙沉淀,同时生成氢氧化钠,可用于除杂,故D正确.
故答案为:AD.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,把握实验的严密性和可行性的评价,注意除杂时不能引入新杂质,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 除去苯中的苯酚可以加入过量浓溴水后过滤 | |
| B. | 向浓硫酸中缓慢加入乙醇和冰醋酸用以制备乙酸乙酯 | |
| C. | 向2mL 10% NaOH溶液中,加入2mL 2mol/L CuSO4溶液,振荡制Cu(OH)2悬浊液,用于检验醛的性质 | |
| D. | 加入Mg(OH)2固体可除去MgCl2溶液中混有的少量FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
| ② |
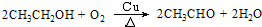 .欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.
.欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| X | Y | 电解质溶液 | |
| A | Zn | Cu | ZnCl2溶液 |
| B | Cu | Zn | 稀H2SO4 |
| C | Cu | Zn | CuSO4溶液 |
| D | Zn | Zn | CuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
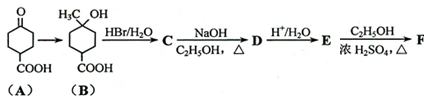
 .①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
.①核磁共振氢谱有2个吸收峰 ②能发生银镜反应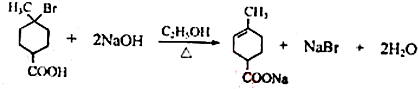 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 草酸二酯的分子式为C26H22Cl6O8 | |
| B. | 1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗6mol NaOH | |
| C. | 草酸二酯酸性条件下水解可以得到两种有机物 | |
| D. | 1mol草酸二酯与氢气完全反应,需要氢气10mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
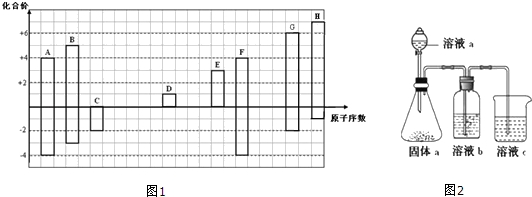
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱:HClO4>H3PO4>H2SO4 | B. | 原子半径大小:Na>P>N | ||
| C. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 | D. | 金属性强弱:K>Na>Li |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com