
����Ŀ������M��һ���ճ������в���ȱ�ٵĵ�ζƷ����֪C����D��ȼ�շ�����ɫ���棬M���������ʵ�ת����ϵ��ͼ��ʾ�����ֲ�������ȥ��

��1��д���ö��Ե缫���M��Һ�����ӷ���ʽ_____��
��2���Ƚ�B�и�Ԫ��ԭ�Ӱ뾶�ɴ�С_____����Ԫ�ط��ţ���
��3����A��һ������������ҿ��������첣������G�Ļ�ѧʽ��_____��
��4����A��һ�ֳ����������ʣ���A��B��Һ�ܹ���Ӧ��������F��Һ��μ���E��Һ���ӱ�����������ʵ��������_____��
��5����A��һ���Σ�A��Һ��B��Һ��ϲ�����ɫ��״������˲���Ϊ����ɫ������ɺ��ɫ��E������Aת����E�����ӷ���ʽ��_____��
��6����A��һ����Һ��ֻ���ܺ���H+��NH4+��Mg2+��Fe3+��Al3+��CO32����SO42���е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ��ʾ���ɴ˿�֪������Һ�п϶����е����Ӽ���Ũ��֮��Ϊ_____��

��7����E�����ڼ��������ǵĴ��ڣ�д��G��Һ����������պ�IJ������Ҵ���Ӧ�Ļ�ѧ����ʽΪ_____��
���𰸡�2Cl��+2H2O![]() 2OH��+H2��+Cl2�� Na��O��H H2SiO3 ��Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ 4Fe2++8OH��+O2+2H2O=4Fe��OH��3�� c��H+����c��Al3+����c��NH4+����c��SO42����=1��1��2��3 CH3CH2OH+CuO
2OH��+H2��+Cl2�� Na��O��H H2SiO3 ��Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ 4Fe2++8OH��+O2+2H2O=4Fe��OH��3�� c��H+����c��Al3+����c��NH4+����c��SO42����=1��1��2��3 CH3CH2OH+CuO![]() CH3CHO+Cu+H2O
CH3CHO+Cu+H2O
��������
��1��C����D��ȼ�շ�����ɫ���棬Ϊ������������Ӧ����HCl������֪CΪH2��DΪCl2��FΪHCl��M���ճ������в���ȱ�ٵĵ�ζƷ����ת����ϵ��֪��M����Һ�������������������B������֪MΪNaCl��BΪNaOH���ö��Ե缫���M��Һ�����ӷ���ʽΪ2Cl��+2H2O![]() 2OH��+H2��+Cl2������2��BΪNaOH��H��O��Na�ֱ�λ��3����ͬ�����ڣ�ԭ�Ӻ�����Ӳ���Խ�࣬ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶��С˳��ΪNa��O��H����3����A��һ�ֳ���������������ҿ��������첣������AΪSiO2��EΪNa2SiO3����F��Һ��Ӧ���Եõ�GΪH2SiO3����4����A��һ�ֳ����������ʣ�����NaOH��Һ�ܹ���Ӧ����AΪAl��EΪNaAlO2��������������Һ��μ���NaAlO2��Һ�У������������������������������ܽ⣬�ʿ���������Ϊ����Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ����5����A��һ���Σ�A��Һ��B��Һ��Ͻ�������ɫ��״������˲���Ϊ����ɫ������ɺ��ɫ��E������֪A�к���Fe2+��EΪFe(OH)3��GΪFeCl3������Aת����E�����ӷ���ʽ�ǣ�4Fe2++8OH��+O2+2H2O=4Fe(OH)3������6����ͼ��֪����ʼ����NaOHû�г����������������һ����H+��һ��û��CO32���������г��������������ʧ����һ��û��Mg2+��Fe3+��һ������Al3+���м�γ������������䣬ӦΪNH4++OH��=NH3H2O�ķ�Ӧ������NH4+���ɵ���غ��֪һ������SO42����������ӦH++OH��=H2O������������NaOH��Һ�����Ϊ1�����������ӦAl3++3OH��=Al(OH)3��������������NaOH��Һ�����Ϊ3�����������ӦNH4++OH��=NH3H2O��笠�������������Ϊ2�������n��H+����n��Al3+����n��NH4+��=1��1��2���ɵ���غ��֪��n��H+����n��Al3+����n��NH4+����n��SO42����=1��1��2��3����c��H+����c��Al3+����c��NH4+����c��SO42����=1��1��2��3����7����E�����ڼ��������ǵĴ��ڣ���EΪ������ͭ��E��F����G����GΪ�Ȼ�ͭ������ͭ������ˮ�⣬�Ȼ����ӷ��������Ȼ�ͭ��Һ����������պ�IJ���Ϊ����ͭ������ͭ���Ҵ�����������ԭ��Ӧ����ͭ����ȩ����Ӧ����ʽΪCH3CH2OH+CuO
2OH��+H2��+Cl2������2��BΪNaOH��H��O��Na�ֱ�λ��3����ͬ�����ڣ�ԭ�Ӻ�����Ӳ���Խ�࣬ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶��С˳��ΪNa��O��H����3����A��һ�ֳ���������������ҿ��������첣������AΪSiO2��EΪNa2SiO3����F��Һ��Ӧ���Եõ�GΪH2SiO3����4����A��һ�ֳ����������ʣ�����NaOH��Һ�ܹ���Ӧ����AΪAl��EΪNaAlO2��������������Һ��μ���NaAlO2��Һ�У������������������������������ܽ⣬�ʿ���������Ϊ����Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ����5����A��һ���Σ�A��Һ��B��Һ��Ͻ�������ɫ��״������˲���Ϊ����ɫ������ɺ��ɫ��E������֪A�к���Fe2+��EΪFe(OH)3��GΪFeCl3������Aת����E�����ӷ���ʽ�ǣ�4Fe2++8OH��+O2+2H2O=4Fe(OH)3������6����ͼ��֪����ʼ����NaOHû�г����������������һ����H+��һ��û��CO32���������г��������������ʧ����һ��û��Mg2+��Fe3+��һ������Al3+���м�γ������������䣬ӦΪNH4++OH��=NH3H2O�ķ�Ӧ������NH4+���ɵ���غ��֪һ������SO42����������ӦH++OH��=H2O������������NaOH��Һ�����Ϊ1�����������ӦAl3++3OH��=Al(OH)3��������������NaOH��Һ�����Ϊ3�����������ӦNH4++OH��=NH3H2O��笠�������������Ϊ2�������n��H+����n��Al3+����n��NH4+��=1��1��2���ɵ���غ��֪��n��H+����n��Al3+����n��NH4+����n��SO42����=1��1��2��3����c��H+����c��Al3+����c��NH4+����c��SO42����=1��1��2��3����7����E�����ڼ��������ǵĴ��ڣ���EΪ������ͭ��E��F����G����GΪ�Ȼ�ͭ������ͭ������ˮ�⣬�Ȼ����ӷ��������Ȼ�ͭ��Һ����������պ�IJ���Ϊ����ͭ������ͭ���Ҵ�����������ԭ��Ӧ����ͭ����ȩ����Ӧ����ʽΪCH3CH2OH+CuO![]() CH3CHO+Cu+H2O��
CH3CHO+Cu+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£�a g�������b g��������ռ���֮��Ϊ1:1�����ݰ����ӵ������жϣ�������������ȷ���ǣ� ��
A.ͬ��ͬѹ�£����ҵ��ܶ�֮��Ϊa:b
B.�����ҵ���Է�������֮��Ϊa:b
C.ͬ��ͬѹ�£�������ļ��ҵ�����֮��Ϊa:b
D.�������ļ����е�ԭ����֮��һ��Ϊb:a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���l L pH=l0��NaOH��Һ�г���ͨ��CO2��ͨ��CO2�����(y)����Һ��ˮ�������c(OH-)�Ĺ�ϵ��ͼ��ʾ�����������������
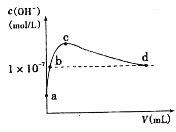
A. a����Һ�У�ˮ�������c(H+)=1��10-10mol��L-1
B. b����Һ�У�c(H+)=1��10-7mol��L-1
C. c����Һ�У�c(Na+)>c(HCO3-)>c(CO32-)
D. d����Һ�У�c(Na+)=2c(CO32-)+c(HCO3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǿ��ƶ���������Ⱦ����Ҫ�����ֶΡ�
��1�����ú�ˮ������һ����Ч�ķ������乤��������ͼ��ʾ��

ij�о�С��Ϊ̽����ߺ���������SO2������Ч�ʵĴ�ʩ����������Ȼ��ˮ���պ���������ģ��ʵ�飬ʵ��������ͼ��ʾ��

�ٸ���ͼʾʵ������Ϊ�����һ��Ũ�Ⱥ���������SO2������Ч�ʣ����д�ʩ��ȷ����___________��
A������ͨ�뺬���������¶� B����Сͨ�뺬������������
C��������Ȼ��ˮ�Ľ����� D������Ȼ��ˮ�м�����ʯ��
����Ȼ��ˮ�����˺��������������H2SO3��ʹ�ÿ����е���������������д���÷�Ӧ�����ӷ���ʽ_____________��
�۸�С�������ͼװ����ʵ���Ҳⶨ������SO2���������������ʵ���ڱ� ״���½��У���

����װ����װ���ӵ�˳���ǣ�ԭ������____����ܽӿ���ţ��������Լ��У�Ũ�ȡ����һ�������������������Թ��еĵ�һ������Һ����____�����ţ���
A.����KMnO4��Һ B.NaOH��Һ C.��ˮ D.��ˮ
��2��ʯ��ʯ-ʯ��ʪ�����������ռ����Ĺ���ԭ���������еĶ��������뽬Һ�е�̼����Լ�����Ŀ�����Ӧ����ʯ��(CaSO4��2H2O)��д���÷�Ӧ�Ļ�ѧ����ʽ��____��ij�糧��ú300t(ú�к�����������Ϊ 2.5%)����ȼ��ʱú�е���ȫ��ת���ɶ��������ø÷�������ʱ��96% ����ת��Ϊʯ�࣬�������ʯ��____t��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ɱ���ܱ������з������·�Ӧ��A(g)+B(g)![]() 2C(g) ��H<0��t1ʱ�̴ﵽƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ������˵����ȷ����
2C(g) ��H<0��t1ʱ�̴ﵽƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ������˵����ȷ����

A. 0��t2ʱ��v������>v���棩
B. t2ʱ�̸ı�����������ǼӴ���
C. �����������̴ﵽ��Ӧ��ʱ��A�����������=��
D. �����������̴ﵽ��Ӧ��ʱ��ƽ�ⳣ��I<��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CO2���ŷ��Լ�CO2����Դ�����þ�����Ҫ���塣
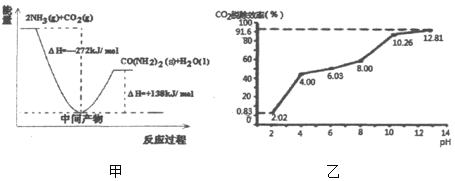
��1��H2NCOONH4�ǹ�ҵ�ϳ�����[CO��NH2��2]���м����÷�Ӧ�������仯ʾ��ͼ��ͼ����ʾ����CO2�Ͱ����ϳ����ص��Ȼ�ѧ����ʽΪ_____��
��2���ð�ˮ���������е�CO2������Σ��Ǽ���CO2�ŷŵĿ��д�ʩ֮һ��
��д����ˮ���������е�CO2����̼����淋���Ҫ��ѧ����ʽ_____��
�ڷֱ��ò�ͬpH�����ռ����������е�CO2��CO2�ѳ�Ч�������ռ���pH��ϵ��ͼ����ʾ��������CO2�ĺ���Ϊ12%������ͨ�백ˮ������Ϊ0.052m3/h����״��������pHΪ12.81�İ�ˮ��������30min���ѳ���CO2�����ʵ������Ϊ_____����ȷ��0.01����
��ͨ��������¶����ߣ�CO2�ѳ�Ч����ߣ�������40��ʱ���ѳ�CO2Ч�ʽ��͵���Ҫԭ����_____��
��3����CO2�ͼ��������ƺϳ�����CO��H2����CO2��Դ�����õ���Ч;�����ϳ��������Ʊ��״��ķ�ӦΪ2H2��g��+CO��g��CH3OH��g����H=��90kJ/mol����T1��ʱ���ݻ���ͬ�ļס��ҡ������������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ��������ͼ��ʾ��
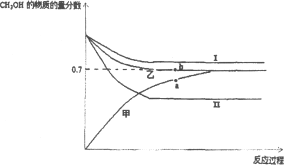
���� | �� | �� | �� |
��ʼ��Ӧ��Ͷ���� | 2molH2��1molCO | 1molCH3OH | 2mol CH3OH |
���ܴ�������Ӧ��������_____��ѡ��I��II����a��b���ѹǿ��ϵΪPa_____Pb���������=����������_____��
��b��ʱ��Ӧ���յ�����Ϊ_____kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������һ����Ҫ��Ӧ�ǣ�CO(g)+H2O(g)CO2(g)+H2(g)����֪��25��ʱ��
C(ʯī)+ 1/2O2(g)=CO(g) ��H=-111kJ/mol
H2(g)+ 1/2O2(g)=H2O(g) ��H=-242kJ/mol
C(ʯī)+O2(g)=CO2(g) ��H=-394kJ/mol
��25��ʱ��1molCO��ˮ��������ת��Ϊ�����Ͷ�����̼��Ӧ����HΪ( )
A. +41kJ/mol B. -41kJ/mol C. -283kJ/mol D. -131kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij100mL��Һ���ܺ���Na+��NH4+��Fe3+��CO32-��SO42-��Cl-�е������֣�ȡ����Һ��������ʵ�飬ʵ�������ͼ��ʾ(�����Լ�������������ȫ���ݳ�)

����˵��һ����ȷ������ ��
A. ��Һ��һ������Na+,Na+Ũ����0.35mol/L
B. ��Һ��ֻ��SO42-��CO32-��NH4+����
C. ��Һ�п��ܺ���Cl-��һ��û��Fe3+
D. ȡԭ��Һ�������������ữ��AgNO3��Һ�����Ƿ���Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʾ������Ԫ���У�W��X��Y��ZΪ������Ԫ�أ�������Ԫ�ص�ԭ������������֮��Ϊ22������˵����ȷ����

A. X��Y��Z����Ԫ����ͼ��⻯��ķе���������
B. ��X��Y��������Ԫ���γɵĻ�������ֻ���й��ۼ�
C. ��X��Y����Ԫ���γɵĻ����ﶼ������������
D. TԪ�صĵ��ʾ��а뵼������ԣ�T��ZԪ�ؿ��γɻ�����TZ4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com