
【题目】Na2O2是一种常见的过氧化物,具有强氧化性和漂白性。 通常可用作漂白剂和呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:

①用化学方程式解释使酚酞试液变红的原因___________________,依据实验现象推测红色褪去的原因是________________。
②加入MnO2的作用为_______________________。
(2)某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:


①写出装置A中反应的化学方程式____________________;
②拟用装置D收集气体产物,请在方框中将装置补充完整______。
③产物检验:检验气体产物的方法:___________________;
④有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么____________。
【答案】2Na2O2 +2H2O = 4 NaOH +O2↑ 反应生成的H2O2具有漂白作用 催化剂的作用 2NaHCO3![]() Na2CO3 + CO2↑ + H2O
Na2CO3 + CO2↑ + H2O ![]() 打开集气瓶,用带火星的木条伸入瓶内,木条复燃 碳酸氢钠受热分解产物中有水,水也与过氧化钠反应,干扰二氧化碳与过氧化钠反应产物的检验
打开集气瓶,用带火星的木条伸入瓶内,木条复燃 碳酸氢钠受热分解产物中有水,水也与过氧化钠反应,干扰二氧化碳与过氧化钠反应产物的检验
【解析】
(1)①过氧化钠和水反应生成碱,碱遇酚酞变红;红色褪去的可能原因是过氧化钠和水反应生成了具有氧化性的过氧化氢;②过氧化氢在二氧化锰的催化作用下分解生成水和氧气;
(2)通过分析可知,装置A为NaHCO3的受热分解,装置B中CO2与Na2O2反应生成O2,同时吸收CO2,装置C检验CO2是否被除尽,装置D收集生成的O2据此判断;
(1)①过氧化钠和水反应生成氢氧化钠和氧气,碱遇酚酞变红;褪色后的溶液中加入二氧化锰产生气泡,红色褪去的可能原因是过氧化钠和水反应生成的过氧化氢具有氧化性;②过氧化氢在二氧化锰的催化作用下分解生成水和氧气;
(2)①NaHCO3受热分解,生成Na2CO3 、CO2和H2O;②NaHCO3分解生成CO2,CO2与Na2O2反应生成O2,经装置C检验,无CO2,装置D收集的是O2,O2密度比空气大,所以用向上排空气法收集氧气,导气管长进短出;③检验O2的方法:打开集气瓶,用带火星的木条伸入瓶内,木条复燃;④通过分析可知存在明显缺陷:碳酸氢钠受热分解产物中有水,水也与过氧化钠反应,干扰二氧化碳与过氧化钠反应产物的检验;


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g) ![]() W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题:
(1)上述反应的化学平衡常数表达式为___________________________。
(2) 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_______;随温度的升高,H2与水蒸气的体积比减小,则该反应为___________反应(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25℃ 550℃ 600℃ 700℃ |
主要成份 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为__________________。
(4)已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) ![]() W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2 ![]() W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
则WO2 (s) ![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) ![]() WI4 (g)。下列说法正确的有________。
WI4 (g)。下列说法正确的有________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应或离子反应方程式正确的是
A. 苯与溴水反应:2![]() +Br2
+Br2![]()
B. 1一氯丙烷中加入氢氧化钠溶液并加热:CH3CH2CH2Cl+NaOH= CH3CH=CH2↑+NaCl+H2O
C. 苯酚钠溶液中通入少量CO2:C6H5O-+H2O+CO2→C6H5OH+HCO3-
D. 实验室制取乙炔的反应:CaC2+H2O → CaO + CH≡CH↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有甲、乙、丙三种物质:
甲![]() 乙
乙 ![]()
分子式 | C9H8O |
部分性质 | 能使Br2/CCl4褪色 |
丙
(1)乙中含有的官能团的名称为_______________;
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
![]()
其中反应II的条件是___,反应III的化学方程式为______(不需注明反应条件);
(3)由甲出发合成丙的路线之一如下:

(a)写出反应③化学方程式________;
(b)丙的结构简式为_______________;
(c)D有多种同分异构体,任写其中一种能同时满足下列条件的异构体结构简式_______。
a.苯环上的一氯代物有两种
b.在空气中易被氧化,遇FeCl3溶液显紫色
c.能与Br2/CCl4发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫、氮气、二氧化碳组成的混合气体在同温、同压下与笑气(N 2O)的密度相同,则该 混合气体中二氧化硫、氮气、二氧化碳的质量比为( )
A. 4:5:6 B. 22:1:14
C. 64:35:13 D. 29:8:13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喷气式飞机在对流层中飞行时排放的尾气NO,能进行下列反应:O3→O2+O;NO+O3→NO2+O2,NO2+O→NO+O2,则NO在这些反应中的作用是( )
A.催化剂B.还原剂C.氧化剂D.中间产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长征2号火箭承担运载“神六”的使命。氢化锂、氘化锂、氚化锂可以作为启动长征2号(CZ2F)火箭发射的优良炸药。下列说法正确的是( )
A. LiH、LiD、LiT的摩尔质量之比为1:2:3
B. 它们互称同分异构体
C. H、D、T之间互称同素异形体
D. 它们都是强还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水中过量的氨氮(NH3和NH4+)会导致水体富营养化。某科研小组用NaClO氧化法处理氨氮废水。已知:①HClO的氧化性比NaClO强;②NH3比NH4+更易被氧化;③国家标准要求经处理过的氨氮废水pH要控制在6~9。
(1)pH=1.25时,NaClO可与NH4+反应生成N2等无污染物质,该反应的离子方程式为________。
(2)进水pH对氨氮去除率和出水pH的影响如图所示
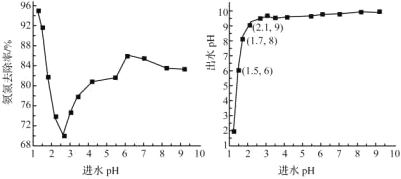
①进水pH为1.25~2.75范围内,氨氮去除率随pH升高迅速下降的原因是_______
②进水pH为2.75~6.00范围内,氨氮去除率随pH升高而上升的原因是______
③进水pH应控制在______左右为宜。
(3)为研究空气对NaClO氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是_______(填字母)。
a.O2的氧化性比NaClO弱 b.O2氧化氨氮速率比NaClO慢
c.O2在溶液中溶解度比较小 d.空气中的N2进入溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《天工开物》中记载:贱者桓裋、枲裳,冬以御寒,夏以蔽体,以自别于禽兽。是故其质则造物之所具也。属草木者为枲、麻、苘、葛,属禽兽与昆虫者裘褐、丝绵。各载其半,而裳服充焉矣。文中的“枲、麻、苘、葛”和“裘褐、丝绵”分别属于( )
A.纤维素、油脂B.糖类、油脂
C.纤维素、蛋白质D.糖类、蛋白质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com