
����Ŀ����ˮ�й����İ���(NH3��NH4+)�ᵼ��ˮ�帻Ӫ������ij����С����NaClO����������������ˮ����֪����HClO�������Ա�NaClOǿ����NH3��NH4+���ױ��������۹��ұ�Ҫ�������İ�����ˮpHҪ������6��9��
��1��pH��1.25ʱ��NaClO����NH4+��Ӧ����N2������Ⱦ���ʣ��÷�Ӧ�����ӷ���ʽΪ________��
��2����ˮpH����ȥ���ʺͳ�ˮpH��Ӱ����ͼ��ʾ
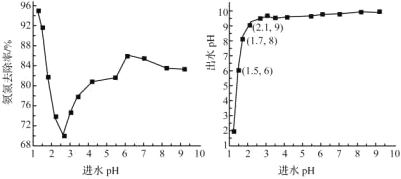
�ٽ�ˮpHΪ1.25��2.75��Χ�ڣ�����ȥ������pH����Ѹ���½���ԭ����_______
�ڽ�ˮpHΪ2.75��6.00��Χ�ڣ�����ȥ������pH���߶�������ԭ����______
�۽�ˮpHӦ������______����Ϊ�ˡ�
��3��Ϊ�о�������NaClO����������Ӱ�죬�����������䣬�����ӵ�λʱ����ͨ��������������ְ���ȥ���ʼ������䡣��ԭ�������_______(����ĸ)��
a��O2�������Ա�NaClO�� b��O2�����������ʱ�NaClO��
c��O2����Һ���ܽ�ȱȽ�С d�������е�N2������Һ��
���𰸡�3ClO����2NH4+=N2����3Cl����3H2O��2H��(��3HClO��2NH4+=N2����3Cl����3H2O��5H��) ����pH���ߣ�NaClO���������������ܽ��ͣ����°���ȥ�����½� ����pH���ߣ�������ˮ��NH3�������������ױ����� 1.50 abc
��������
(1)pH=1.25ʱ��NaClO����NH4+��Ӧ����N2������Ⱦ���ʣ�����������ӱ���ԭΪ�����Ӻ�ˮ����ϵ���غ㡢�����غ㡢ԭ���غ���ƽ��д���ӷ���ʽ��
(2)�ٽ�ˮpHΪ1.25��2.75��Χ�ڣ����HClO�������Ա�NaClOǿ������𣻢ڽ�ˮpHΪ2.75��6.00��Χ�ڽ��NH3��NH4+���ױ�����������𣻢۸���ͼ���Ϸ�ˮ�ŷű������жϣ�
(3)�����������䣬�����ӵ�λʱ����ͨ��������������ְ���ȥ���ʼ������䣬˵��O2�����������ʱ�NaClO�����ȴ�������������������Һ���ܽ�������ٵ�ԭ��
(1)pH=1.25ʱ��NaClO����NH4+��Ӧ����N2������Ⱦ���ʣ�����������ӱ���ԭΪ�����ӣ���ϵ���غ㡢�����غ㡢ԭ���غ���ƽ��д���ӷ���ʽ��3ClO����2NH4+=N2����3Cl����3H2O��2H�����ʴ�Ϊ��3ClO����2NH4+=N2����3Cl����3H2O��2H����
(2)�ٽ�ˮpHΪ1.25��2.75��Χ�ڣ�����pH���ߣ�HClO�������ͣ�NaClO�ĺ������ߣ�����HClO�������Ա�NaClOǿ��NaClO���������������ܽ��ͣ����°���ȥ�����½����ʴ�Ϊ������pH���ߣ�NaClO���������������ܽ��ͣ����°���ȥ�����½���
�ڽ�ˮpHΪ2.75��6.00��Χ�ڣ�����pH���ߣ�������ˮ�а���������������NH3��NH4+���ױ�������ʹ�ð������ױ��������ʴ�Ϊ������pH���߰�����ˮ�а����������������ױ�������
�۸���ͼʾ����Ϲ��ұ�Ҫ�������İ�����ˮpHҪ������6��9����ˮpHӦ������1.50���ң�����ȥ���ʻ�ϴ������İ�����ˮpH��6���ң������ŷű����ʴ�Ϊ��1.50��
(3)�о�������NaClO����������Ӱ�죬�����������䣬�����ӵ�λʱ����ͨ��������������ְ���ȥ���ʼ������䡣��ԭ������ǣ�O2�������Ա�NaClO����O2�����������ʱ�NaClO����O2����Һ���ܽ�ȱȽ�С���ʴ�Ϊ��abc��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�һ������Ũ����������ͭ��ȫ��Ӧ���õ�����ͭ��Һ��NO2��NO�Ļ������2.24L����״��������Щ������һ�������O2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���4mol.L-1NaOH��Һ��Cu2+ǡ����ȫ������������NaOH��Һ�������50mL,����˵����ȷ����
A. �μӷ�Ӧ��������0.4mol B. �������������Ϊ1.68L
C. ��������к�NO2 1.12L D. �˷�Ӧ������ת�Ƶĵ���Ϊ0.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2O2��һ�ֳ����Ĺ����������ǿ�����Ժ�Ư���ԡ� ͨ��������Ư���ͺ�������еĹ�������
��1��ijʵ��С��ͨ������ʵ��̽������������ˮ�ķ�Ӧ��

������ѧ����ʽ����ʹ��̪��Һ����ԭ��___________________������ʵ�������Ʋ��ɫ��ȥ��ԭ����________________��
�ڼ���MnO2������Ϊ_______________________��
��2��ijʵ��С������֤CO2��Na2O2��Ӧ�IJ�����������ʵ��װ�ý���ʵ�飺


��д��װ��A�з�Ӧ�Ļ�ѧ����ʽ____________________��
������װ��D�ռ����������ڷ����н�װ�ò�������______��
�۲�����飺�����������ķ�����___________________��
����ͬѧ��Ϊ��ʵ��װ�ô�������ȱ�ݣ�����Ϊ��ȱ����ʲô____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д��ȷ����
A��̼��ĵ��뷽��ʽ��H2CO3 ![]() 2H+ + CO32��
2H+ + CO32��
B. ����ˮ��: S2-+2H2O![]() H2S +2OH-
H2S +2OH-
C����AgI����Һ�еμ�Na2S������Һ��2Ag+ (aq)+ S2��(aq) = Ag2S(s)
D���ô����ˮ���� 2CH3COOH + CaCO3 = 2CH3COO- + Ca2+ + H2O + CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2H2O2��l���T2H2O��l��+O2��g����Ӧ�����е������仯������ͼ��ʾ������˵������ȷ����

A. ;������;������ȣ������Ǽ����˶�������
B. 2molH2O2��l������������2molH2O��l��������
C. ����������ͬ��������ͬ������ʱ�ų���������;�������;����
D. ����������ͬ��������ͬ��������ʱ��;�������;����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��X��Q��Y��Z��M��R��Ϊ����������Ԫ�أ���ԭ����������������֪Yԭ������������������������֮��Ϊ3��4��Mԭ�ӵ����������������������֮��Ϊ3��4��R����Z����X�����Ӱ뾶��С��������XR������Ϊ���壬Q��Y�����ڱ��е�λ�����ڣ���ش��������⣺
��1��д������R��һ�ֹ�ҵ��;_______________________��
��2��M��R������������ˮ������������ǿ����___________���û�ѧʽ��ʾ����
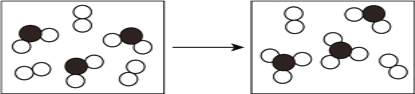
��3����ͼ��ʾ������Ԫ���е�ij����Ԫ����ɵ����������һ�������µ��ܱ������г�ַ�Ӧǰ���ת����ϵ��д����ת�����̵Ļ�ѧ����ʽΪ____________________��
��4����X��Y��Z��M����Ԫ����ɵ�һ�����ӻ�����A����֪A�����������ᷴӦ������������������Һ��Ӧ�����ܺ���ˮ��Ӧ��д��A����ˮ��Ӧ�����ӷ���ʽ___________��
��5����ѧ����Ϊ����QX5�������ʣ���Ԥ������ˮ���ҷ�Ӧ�ų����壬����ˮ��Һ�������ԣ���֪QX5�к������Ӽ��ͼ��Լ���д��������ĵ���ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶������ݻ�������ܱ������У��������¿��淴Ӧ��H2(g)+CO2(g)![]() CO(g)+H2O(g)�������ܱ����÷�Ӧ�Ѵﵽƽ��״̬���� ( )
CO(g)+H2O(g)�������ܱ����÷�Ӧ�Ѵﵽƽ��״̬���� ( )
A. ���������ܶȱ��ֲ���
B. �����е�ѹǿ���ֲ���
C. ����(CO2)=����(CO)
D. CO��H2O�����ʵ���Ũ��֮�Ȳ���ʱ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��SO2����Ҫ�Ĵ�����Ⱦ���壬���û�ѧ��Ӧԭ����������Ⱦ����Ҫ������
�����״����Բ���Ͳ������ʯ��ȼ�ϣ�������Դ���ţ�����CO���Ժϳɼ״���
��1����֪��CO(g)+1/2O2(g)�TCO2(g)��H1=-283.0kJ��mol��1
H2(g)+1/2O2(g)�TH2O(l)��H2=-285.8kJ��mol��1
CH3OH(g)+3/2O2(g)�TCO2(g)+2H2O(l)��H3=-764.6 kJ��mol��1
��д��CO��H2�ϳɼ״��������Ȼ�ѧ����ʽ____________________
��2��һ�������£����ܼ�ΪVL���ܱ������г���a molCO��2a molH2�ϳɼ״���ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

�ٸ÷�Ӧ��A���ƽ�ⳣ��K=_________________(��a��V��ʾ)
��������˵����Ӧ�ﵽƽ��״̬����_____
A.v(CO)=v(H2) B.���������ܶȲ���
C.��������ƽ����Է����������� D. c(CO)=c(H2)
��д��������v(CO)�������COת���ʵ�һ���ʩ_____________________________
����ijѧϰС����SO2Ϊԭ�ϣ����õ绯ѧ������ȡ���ᡣ
��3��ԭ���ԭ������С����Ƶ�ԭ��ʾ��ͼ������ͼ��д���õ�ظ����ĵ缫��Ӧʽ______��
��4�����ԭ������С����Na2SO3��Һ�������SO2�õ�NaHSO3��Һ��Ȼ�������Һ�Ƶ������ᡣԭ����ͼ��д����ʼ���ʱ�����ĵ缫��Ӧʽ________________��


��5����֪25��ʱ��Na2SO3��NaHSO3�γɵĻ����Һǡ�ó����ԣ���û����Һ�и�����Ũ�ȵĴ�С˳��Ϊ________________________________(��֪25��ʱ��H2SO3�ĵ���ƽ�ⳣ��Ka1=1��10-2��Ka2=1��10-7)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�������д��ȷ����
A. ����ķ���ʽ��C2H4O2B. ��ϩ�Ľṹ��ʽ C2H4
C. Fԭ�ӽṹʾ��ͼ�� D. ���Ȼ�̼�ĵ���ʽ��
D. ���Ȼ�̼�ĵ���ʽ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com