
【题目】下列物质与水反应生成强碱的是( )
A. NH3 B. Na2O C. CO2 D. NO2
【答案】B
【解析】
A. NH3溶于水生成一水合氨,属于弱碱,A错误;B. Na2O溶于水生成氢氧化钠,是强碱,B正确;C. CO2溶于水生成碳酸,属于弱酸,C错误;D. NO2溶于水生成硝酸和NO,硝酸是强酸,D错误,答案选B。
【题型】单选题
【结束】
19
【题目】利用下列装置可以完成的实验组合是

选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 浓硫酸 | H2 |
D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
A. AB. BC. CD. D
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液,进行以下实验探究。

(1)图一是根据反应Zn + CuSO4 == Cu + ZnSO4 设计成的锌铜原电池。Cu极的电极反应式是________________________________________,盐桥中是含有琼胶的KCl饱和溶液,电池工作时K+向_______移动(填“甲”或“乙”)。
(2)图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是________(填“CH4”或“O2”),a处电极上发生的电极反应式是__________________________________________;当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为________________L。
(3)一段时间后,燃料电池的电解质溶液完全转化为K2CO3,以下关系正确的是______________。
A.c(K+)+c(H+)=c(HCO3-)+ c(CO32-)+c(OH-)
B.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C.c(K+)>c(CO32-)>c(H+)>c(OH-)
D.c(K+)>c(CO32-)>c(OH-)>c(HCO3-)
E.c(K+)= 2c(CO32-)+ c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有镁、铝合金5.1g完全溶于稀盐酸中,在标准状况下共收集到氢气5.6L,计算:
(1)氢气的物质的量是 。
(2)双线桥法表示出铝和盐酸反应的电子转移的方向和数目?
(3)求这种合金中镁、铝的物质的量分别是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如下表:
H2CO3 | H2SO3 | HClO |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
K2=5.61×10-11 | K2=1.02×10-7 |
下列说法正确的是
A. 相同条件下,同浓度的 H2SO3溶液和 H2CO3溶液的酸性, 后者更强
B. Na2CO3溶液中通入少量SO2: 2CO3 2- + SO2+ H2O = 2HCO3 - + SO3 2-
C. NaClO 溶液中通入少量CO2:2ClO- + CO2 + H2O = 2HClO + CO3 2-
D. 向氯水中分别加入等浓度的 NaHCO3 和 NaHSO3溶液,均可提高氯水中 HClO 的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分子式为C7H8的芳香烃在镍的催化下与足量氢气加成后生成环烷烃,请写出该环烷烃的一氯代物的结构简式:______、______、_______、_______、_______。
(2)烷烃C8H18的一种同分异构体只生成一种一氯代物,试写出这种异构体的结构简式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上的电子数是原子核外电子层数的2倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
Z | 元素最高正价是+7价 |
完成下列问题:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是________。
(2)元素Y与氢元素形成一种分子YH3,写出该粒子的电子式________。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明的是________。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(4)T、X、Z三种元素最高价氧化物的水化物酸性由强到弱的顺序是_____(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
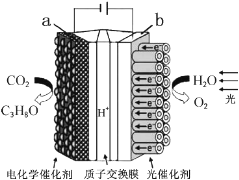
A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1molO2,有44g CO2被还原
D. a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com