
【题目】下列各组离子能在呈酸性的无色溶滚中大量共存的是( )
A. Ba2+、Na+、NO3-、SO42- B. Mg2+、Cl-、Al3+、SO42-
C. K+\、OH-、HCO3-、NO3- D. NH4+、Na+、Fe2+、MnO4-
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】硫化锌荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方硫化锌的晶胞如图所示。请回答下列问题:

(1)锌元素在周期表中的位于第______周期_____族, 属于_____区;
(2)基态锌原子的价电子排布式为_________;
(3)一般锌元素常表现为+2 价的原因是_____;
(4)立方硫化锌晶体的每个晶胞中含有_____个锌离子, 其配位数为_____;含有_____个硫离子,其配位数为_____;
(5)根据神奇的“百度”显示,该晶胞的棱长a=541pm,S2-的半径约为184pm,则 Zn2+在此晶胞中的半径大约为______pm(精确到1pm)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.
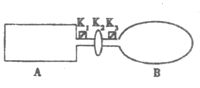
关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应开始时,A、B的体积相同。已知:2NO2(g)![]() N2O4(g) △H<0。
N2O4(g) △H<0。
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是V(A) V(B)(填“<”、“>”或“=”);若打开活塞K2,气球B将 (填“变大”、“变小”或“不 变”,下同)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将 。
若通入等量的Ne气,则达到平衡时,A中NO2的转化率将 ,B中NO2的转化率将 。
(3)室温时,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深。
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的压强为原来的80%,试求出平衡时NO2的转化率(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
① CH4(g) = C(s)+2H2(g) △H= + 75.0 kJ·mol—1
② CO2(g)+H2(g)= CO(g)+H2O(g) △H = + 41.0 kJ·mol—1
③ CO(g)+H2(g) = C(s)+H2O(g) △H = -131.0 kJ·mol—1
反应CO2(g)+CH4(g) = 2CO(g)+2H2(g)的△H =___________kJ·mol—1。
II.用CO合成尿素的反应为:2NH3(g) + CO(g)![]() CO(NH2)2(g) + H2(g) ΔH <0。
CO(NH2)2(g) + H2(g) ΔH <0。
(1)T ℃时,向体积为2 L的恒容密闭容器中,充入2 molNH3和1 mol CO发生反应。
① 5 min时反应达到平衡状态,CO的转化率为80%,则5 min内NH3的平均反应速率为________,此温度下反应的平衡常数K的值为 ____________ 。
②对该反应,下列说法正确的是______(填字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.反应达到平衡后,其它条件不变,升高温度,尿素的百分含量增大
C.反应达到平衡后,其它条件不变,在原容器中充入一定量氦气,CO的转化率不变
D.反应达到平衡后,其它条件不变,充入一定量NH3,平衡向正反应方向移动,但K值不变
(2)若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:若图中c表示平衡体系中尿素的体积分数,则b表示________的转化率。当尿素含量最大时,则![]() =______,此时,对于该反应既能增大反应速率又能提高尿素体积分数的措施为_____。
=______,此时,对于该反应既能增大反应速率又能提高尿素体积分数的措施为_____。

Ⅲ.下图是铬酸银(Ag2CrO4)T ℃时,在水溶液中的沉淀溶解平衡曲线。

(1)向饱和Ag2CrO4溶液中加入固体K2CrO4______(填“能”或“不能”)使溶液由Y点变为X点
(2)图中ɑ = _________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)2HBr(g);△H<0. 当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )

A. 由图可知:T1>T2
B. a、b两点的反应速率:b>a
C. 为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法
D. T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A.不能让小学生咬铅笔头,否则会引起铅中毒
B.食用碱用于面包加工,可以使面包疏松
C .铝合金用作门窗框架,这是利用了合金硬度大的特征
D.烧碱和冰醋酸均为电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学与自然资源的开发利用说法中不正确的是
A. 海水提镁的过程为:MgCl2(aq)![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 铝热反应实验中,需要用到的试剂有镁条、氯酸钾、铝粉和铁的氧化物
C. 电解法制备铝的化学方程式为:2Al2O3 ![]() 4Al + 3O2↑
4Al + 3O2↑
D. 金属铜的制备一般用热还原法:H2 + CuO ![]() Cu + H2O
Cu + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol·L-1H3PO2溶液中滴加0.1mol·L-1的NaOH溶液,滴定曲线如图1,含磷微粒物质的量浓度所占分数(δ)随pH变化关系如图2。下列说法不正确是

A. H3PO2的电离方程式为H3PO2![]() H2PO2-+H+ Ka≈10-5
H2PO2-+H+ Ka≈10-5
B. B点时,溶液中存在关系:2c(H+)+c(H2PO2-)=2c(OH-)+c(H3PO2)
C. C点时,溶液中存在关系:c(Na+)+c(H+)=C(H2PO2-)+c(OH-)
D. D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com