
【题目】25℃时,向20mL0.1mol·L-1H3PO2溶液中滴加0.1mol·L-1的NaOH溶液,滴定曲线如图1,含磷微粒物质的量浓度所占分数(δ)随pH变化关系如图2。下列说法不正确是

A. H3PO2的电离方程式为H3PO2![]() H2PO2-+H+ Ka≈10-5
H2PO2-+H+ Ka≈10-5
B. B点时,溶液中存在关系:2c(H+)+c(H2PO2-)=2c(OH-)+c(H3PO2)
C. C点时,溶液中存在关系:c(Na+)+c(H+)=C(H2PO2-)+c(OH-)
D. D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
科目:高中化学 来源: 题型:
【题目】下列各组离子能在呈酸性的无色溶滚中大量共存的是( )
A. Ba2+、Na+、NO3-、SO42- B. Mg2+、Cl-、Al3+、SO42-
C. K+\、OH-、HCO3-、NO3- D. NH4+、Na+、Fe2+、MnO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2NO2(g)![]() 2NO(g)+O2(g)在恒容密闭容器中进行,达到平衡状态的标志是
2NO(g)+O2(g)在恒容密闭容器中进行,达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO
②单位时间内生成n molO2的同时生成2n mol NO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
A. ①③⑤ B. ②④⑥ C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物F 和J的合成路线如下:

已知:
1 乙烯醇不稳定,会迅速转化为乙醛
2 CH2=CH2+1/2O2+CH3COOH-----CH2=CHOOCCH3+H2O
3 
(1)G中官能团的名称是_________________。
(2)C的结构简式是_____________________。
(3)芳香烃D的一氯代物只有两种,则D的结构简式是___________________。
(4)反应③的反应类型是___________________。
(5)反应②和⑤的化学方程式分别是:
反应②_________________;_______________
反应⑤_________________________________。
(6) E也可由A和2,4-己二烯为原料制备,请写出该合成路线______________(无机试剂任选)。
E也可由A和2,4-己二烯为原料制备,请写出该合成路线______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)

实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15 mL甲苯(密度为0.866 g·cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,大约反应10分钟至三颈烧瓶底有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15 g.
根据上述实验,回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,则会产生__________等副产品(填物质名称)
(2)简述配制混酸的方法:____________________.
(3)A仪器名称是__________,进水口是__________.
(4)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:___________________________.
(5)分离产品方案如下:

操作2的名称是___________.经测定,产品2的核磁共振氢谱中有5个峰,它的名称为___________.
(6)本实验中一硝基甲苯的产率为___________ (结果保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里做钠跟水反应的实验时,用到的仪器和药品是:①试管夹、②镊子、③小刀、④滤纸、⑤研钵、⑥烧杯、⑦坩埚、⑧石棉网、⑨玻璃片、⑩药匙.
A.①②③④ B.②③④⑥⑨ C.③④⑧⑨⑩ D.②⑤⑦⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)五种元素。
请回答下列问题:
(1)①与氧同周期的相邻元素及氧的第一电离能由大到小的顺序为________________。
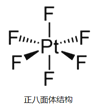
②已知:离子型配位化合物O2[PtF6]中铂元素为+ 5价,它可由反应PtF6+O2= O2[PtF6]制得,PtF6分子结构如图所示。PtF6分子中Pt的杂化轨道类型是否为sp3?答:_____(填“是”或“否”),其原因是_______。
(2)臭鼬排放的臭气主要成分为3-MBT(3-甲基-2-丁烯硫醇,结构简式为![]() )。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
)。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
(3)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法中正确的是_____(填字母)。
A.中心原子的价层电子对数目相等
B.都是极性分子
C.中心原子的孤对电子数目相等
D.都含有极性键
②SO3子的空间构型为________,与其互为等电子体的阴离子为_____(举一例)。
(4)元素X与硒同周期,且该周期中X元素原子核外未成对电子数最多,则X为____基态原子的电子排布式为_______。
(5)单质钋是由_____键形成的晶体,其晶胞为简单立方;若已知Po的摩尔质量为Mg·mol-1,原子半径为rpm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为_____g·cm-3(只列表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,下图是利用一种微生物将废水中的尿素[CO(NH2)2]转化为对环境无害物质的装置。下列叙述错误的是

A. M电极有CO2和N2生成
B. H+透过质子交换膜由左向右移动
C. 微生物促进了反应中电子的转移
D. N电极反应式为O2 + 2H2O + 4e﹣= 4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com