
| A、①② | B、②③ | C、③ | D、④ |


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
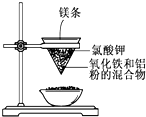 用如图所示的装置进行实验,回答下列问题:
用如图所示的装置进行实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对废旧金属的最好处理方法是回收、再用 |
| B、提炼金属要经过矿石的富集、冶炼、精炼三步 |
| C、活泼金属的冶炼都是通过电解其盐溶液 |
| D、热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铵分子中含有一个NH4+和一个Cl- |
| B、氯化铵由N、H、Cl三种元素组成 |
| C、氯化铵晶体由NH4+和Cl-构成 |
| D、氯化铵晶体中阴、阳离子个数比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
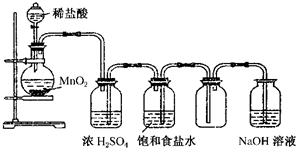
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度下,pH=6的纯水中含有OH-的数目为10-6 NA |
| B、120 g NaHSO4固体中含有的离子总数为2NA |
| C、1L0.1mol?L-1氨水含有0.1NA个OH- |
| D、1mol甲醇中含有C-H键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+3H+═2Na++H2↑ |
| B、Na+H2O═Na++OH-+H2↑ |
| C、2Na+2H2O═2Na++2OH-+H2↑ |
| D、2Na+2H2O═2Na++O2↑+2H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com