
| n |
| V |


科目:高中化学 来源: 题型:
| A、用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O |
| B、过氧化钠加到冷水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| C、少量氢氧化钠溶液与氯化铝溶液反应:Al3++3OH-=Al(OH)3↓ |
| D、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴 | B、水 |
| C、溴水 | D、溴蒸气和液溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从海水中可以得到NaCl,电解熔融NaCl可制备金属Na |
| B、海水蒸发制海盐的过程中只发生了化学变化 |
| C、海水的淡化,只需经过化学变化就可以得到 |
| D、利用海水、铝、空气的航标灯的原理是将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应物物质的量之间的关系 | 此阶段被氧化的离子的符号 | 被氧化离子的物质的量 | ||||
| 0<c≤a | ① | ② | ||||
a<c≤
| ③ | ④ | ||||
| ⑤ | ⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
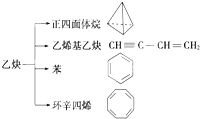 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A、正四面体烷的分子式为C4H4,其二氯代物只有一种 |
| B、等物质的量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 |
| C、苯为平面六边形结构,分子中存在C-C和C═C |
| D、环辛四烯跟苯的结构很像,所有原子在同一平面,不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com