
| 反应物物质的量之间的关系 | 此阶段被氧化的离子的符号 | 被氧化离子的物质的量 | ||||
| 0<c≤a | ① | ② | ||||
a<c≤
| ③ | ④ | ||||
| ⑤ | ⑥ |
| a+b |
| 2 |
| 3a+b |
| 2 |
| 3a+b |
| 2 |
| 3(a+b) |
| 2 |
| 3a+b |
| 2 |


科目:高中化学 来源: 题型:
| A、NH3?H2O═NH4++OH- |
| B、CuCl2═Cu2++Cl- |
| C、H2CO3═2H++CO32- |
| D、NaOH═Na++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氯乙烷存在二种同分异构体 |
| B、油脂在酸性条件下的水解产物都能与金属钠反应 |
| C、除去乙酸乙酯中少量的乙酸,用饱和碳酸钠溶液洗涤后分液 |
| D、等物质的量的甲烷与氯气混合气,在光照条件下生成的产物物质的量也相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/LCH3COOH与1mol/L CH3COONa溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA |
| B、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+ |
| C、AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 |
| D、常温下,0.01mol?L-1醋酸溶液与等体积0.02 mol?L-1NaNO3溶液混合后有:2c (NO3-)═c (CH3COO-)+c (CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对废旧金属的最好处理方法是回收、再用 |
| B、提炼金属要经过矿石的富集、冶炼、精炼三步 |
| C、活泼金属的冶炼都是通过电解其盐溶液 |
| D、热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、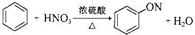 | |||
| B、H2C=CH2+Br2→CH3CHBr2 | |||
C、CH3COOH+CH3CH2OH
| |||
D、CH4+2O2
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com