
【题目】某原电池总反应为:Cu+2Fe3+==Cu2++2Fe2+,下列能实现该反应的原电池是
A | B | C | D | |
电极材料 | Cu、C | Cu、Ag | Cu、Zn | Fe、Zn |
电解质溶液 | Fe(NO3)3 | FeSO4 | FeCl3 | CuSO4 |
A. A B. B C. C D. D
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是( )
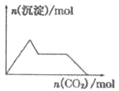
A. 含0.0l mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2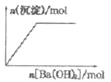
B. NaHSO4溶液中逐滴加入Ba(OH)2溶液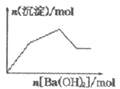
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液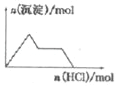
D. NaAlO2溶液中逐滴加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
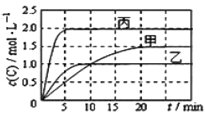
容器 | 甲 | 乙 | 丙 |
容积 | 1L | 1L | 2L |
温度/℃ | T1 | T2 | T2 |
反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是( )
A. 由图可知Tl<T2,且正反应为吸热反应
B. 前5min内甲、乙、丙三个容器中反应的平均速率:v (A)乙<v(A)甲<v(A)丙
C. 平衡时A的转化率a : a乙<a甲<a丙
D. T2时该反应的平衡常数K=1.33
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式相对应的化学方程式正确的是 ( )
A. Cu2+ + 2OH- = Cu(OH)2↓ CuCO3 + 2NaOH = Cu(OH)2↓ + Na2CO3
B. Ba2+ + SO42- = BaSO4↓ Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O
C. Ag+ + Cl- = AgCl↓ AgNO3 + NaCl = AgCl↓ + NaNO3
D. Cu + 2Ag+ = Cu2++2Ag↓ Cu + 2AgCl=2Ag + CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某固定体积的绝热密闭容器中进行的可逆反应A (g)+B(g)![]() C(s)+2D(g),可以说明己达到平衡状态的是( )
C(s)+2D(g),可以说明己达到平衡状态的是( )
①反应容器中压强不随时间变化而变化;②A气体和B气体的生成速率相等;③混合气体的平均摩尔质量不随时间变化而变化;④混合气体的密度不随时间变化而变化⑤化学平衡常数不变
A. ①④⑤ B. ③④ C. ①③④⑤ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制500 mL0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为____________。(精确到0.1g)
(2)有以下仪器:①烧杯 ②100ml量筒 ③1000ml容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦滴定管
(Ⅰ)配制时,必须使用的仪器有_____(填代号),还缺少的仪器是__;
(Ⅱ)实验两次用到玻璃棒,其作用分别是:______________、_____________。
(Ⅲ)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_______________
(3)某学生实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是_______。
A.使用滤纸称量氢氧化钠固体
B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤
D.胶头滴管加水定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】)常温下钛的化学活性很小,在较高温度下可与多种物质反应。
(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:

① 沸腾氯化炉中发生的主要反应为:_____________。
② 己知:Ti (s)+2Cl2(g)=TiCl4(l) △H=akJ/mol;
2Na(s)+Cl2(g)=2NaCl(s) △H=bkJ/mol;
Na(s) = Na (l) △H=ckJ/mol
则TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s) △H=________kJ/mol
③ TiCl4遇水强烈水解,写出其水解的化学方程式________。
(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示。二氧化钛电极连接电源_____极,该极电极反应为__________。

(3)若以二甲醚(CH3OCH3)、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是( )
A.天然气在空气中燃烧的反应 B.灼热的木炭与CO2的反应
C.铁粉与稀硫酸的反应 D.Ba(OH)2 8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com