
【题目】下列示意图与对应的反应情况正确的是( )
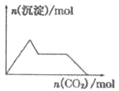
A. 含0.0l mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2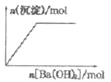
B. NaHSO4溶液中逐滴加入Ba(OH)2溶液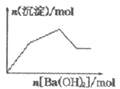
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液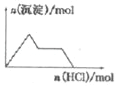
D. NaAlO2溶液中逐滴加入盐酸
【答案】B
【解析】A、向一定量的氢氧化钙和氢氧化钾溶液中通入二氧化碳,开始先和氢氧化钙反应,会逐渐生成碳酸钙沉淀,沉淀量逐渐增大,当氢氧化钙完全反应后,再和氢氧化钾反应,此时沉淀量不变,当氢氧化钾消耗完毕时,将碳酸钙逐渐溶解,沉淀量逐渐减少,故A错误;
B、NaHSO4溶液中逐滴加入Ba(OH)2溶液会产生越来越多的硫酸钡白色沉淀,直到最大量,然后不再减少,沉淀的量保持不变,故B正确;
C、假设含2molKAl(SO4)2溶液中逐滴加入Ba(OH)2溶液,开始阶段滴加入3molBa(OH)2时,2mol铝离子和3mol硫酸根分别和氢氧根和钡离子反应生成2mol氢氧化铝和3mol硫酸钡沉淀共5mol沉淀,然后再滴加入1molBa(OH)2时,继续形成1mol的硫酸钡沉淀但同时有会溶解2mol氢氧化铝沉淀,所以这一段沉淀的物质的量并没有增多反而减小,再滴加入Ba(OH)2时无反应发生最终只剩余硫酸钡沉淀,故C错误;
D、NaAlO2溶液中逐滴加入盐酸,开始出现沉淀,然后过量的盐酸又将沉淀逐渐溶解掉,故D错误.
故选B.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,欲测定Na2O2试样的纯度。可供选用的反应物只有CaCO3固体、6mol·L-1硫酸、6mol·L-1盐酸和蒸馏水。已知:①浓硫酸有吸水性、脱水性和强氧化性,②碱石灰的成分为CaO和NaOH。实验方案为:①制备并提纯CO2。②将纯净的CO2通过试样。③测定生成O2的体积。④根据O2的体积计算Na2O2试样的纯度。实验装置如下:

回答下列问题:
(1)装置A中发生反应的离子方程式是______________________________________。
(2)装置B的作用是_______________________,装置C的作用是_______。
(3)装置E的作用是__________________________________________
(4)装置D中发生反应的化学方程式是______________________________________。
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 标准状况下,11.2LSO2气体中含氧原子数等于18g水中含有的氧原子数
B. 5.6 g铁与足量稀硫酸反应失去的电子的物质的最为0.3 mol
C. 100g98%的浓硫酸所含的氧原子个数为4mol
D. 20gNaOH溶于1L水,所得溶液中c(Na+)=0.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42-、CO32-。为了进一步确认,对该溶液进行实验检测:

实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无________。 | 肯定无该离子的理由______________。 |
步骤二 | 该溶液呈无色、透明、均一状态; | 肯定无________。 | 肯定无该离子的理由______________。 |
(1)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、 _________、干燥、在干燥器中冷却。
(2)原溶液中H+物质的量浓度为 __________mol/L。
(3)向溶液中加入NaHCO3溶液,反应的离子方程式为:____________________________。
(4)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,当Mg2+恰好沉淀完全时加入的Ba(OH)2溶液体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钙可用作阻燃剂、制冷剂,具有易溶于水,易吸潮等性质.实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:

经查阅资料:①HBr(氢溴酸)为一元强酸;
②Al3+、Fe3+在pH=8时完全转化为沉淀。
③V为IV过滤后的溶液。
(1)写出I溶解的离子方程式:_________________________________________。
(2)上述使用的氢溴酸的质量分数为26%,若用47%的氢溴酸(密度为1.49g/cm)配置26%的氢溴酸500 mL,所需的玻璃仪器有玻璃棒、胶头滴管、___________。
(3)已知步骤Ⅲ的滤液中不含NH4+.步骤Ⅱ加入的试剂a是_____________(填化学式)。
A.NaOH B. Ba(OH)2 C. NH3·H2O D. Ca(OH)2
(4)步骤Ⅴ所含的操作依次是__________________、__________________、过滤。
(5)制得的溴化钙可以通过如下步骤测定其纯度:
①称取4.00g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤;④烘干,冷却。⑤称量.若得到1.88g碳酸钙,则溴化钙的质量分数为_________________ (保留两位小数),若实验操作规范而测定结果偏低,其原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们发现PtCl2(NH3)2有两种不同性质的异构体,性质如下表:请回答下列问题:
配合物 | 颜色 | 在水中的溶解 | 抗癌活性 |
PtCl2(NH3)2 | 黄绿色 | 0.2577g/100gH2O | 有活性 |
PtCl2(NH3)2 | 淡黄色 | 0.0360g/100gH2O | 无活性 |
(1)PtCl2(NH3)2的空间结构是______________;
(2)根据它们的性质分析,淡黄色固体是________________(填“极性分子”或“非极性分子”)。
(3)请画出黄绿色固体分子的几何构型图:__________________;
(4)黄绿色固体在水中溶解度较大的原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应为:Cu+2Fe3+==Cu2++2Fe2+,下列能实现该反应的原电池是
A | B | C | D | |
电极材料 | Cu、C | Cu、Ag | Cu、Zn | Fe、Zn |
电解质溶液 | Fe(NO3)3 | FeSO4 | FeCl3 | CuSO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示: 下列有关说法正确的是

A.该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.沉淀乙一定有BaCO3,可能有BaSO4
D.一定没有Fe3+,但是无法确定是否含有I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com